Поступило в редакцию: Февраль 2024
УДК 54:001.8(470)
Fluorine Notes, 2024, 153, 3-4
СИНТЕЗ И ЯМР ИССЛЕДОВАНИЕ ПРОДУКТА N‑ПОЛИФТОРАЛКИЛИРОВАНИЯ ТРИС(2-АМИНОЭТИЛ)АМИНА 1Н,1Н,9Н-ТРИГИДРОПЕРФТОРНОНАН-1-ОЛОМ
С. В. Кудашев1, В. С. Сидельников2,3, И. А. Полицимако1, В. Ф. Желтобрюхов1
1Волгоградский государственный технический университет, 400005 Россия, Волгоград, проспект Ленина, 28
e-mail: kudashev-sv@yandex.ru
2Национальный исследовательский Томский государственный университет, 634050 Россия, Томск, проспект Ленина, 36
3Томский региональный центр коллективного пользования (ТРЦКП), Томского государственного университета, 634050 Россия, Томск, проспект Ленина, 36
Аннотация: Взаимодействием трис(2-аминоэтил)амина с полифторированным спиртом в присутствии каталитических количеств монтмориллонитовой глины синтезирован соответствующий продукт N-полифторалкилирования. Методами одномерной (1H, 13C, 19F) и двумерной гетероядерной (1H-15N HMBC) ЯМР спектроскопии исследована структура полученного соединения.
Ключевые слова: полифторированный спирт, полиэтиленполиамины, катализ, ЯМР спектроскопия, алкилирование, монтмориллонит.
Введение
Синтез фторированных аминов [1-3] представляет интерес в связи с возможностью их применения в качестве реагентов для получения биологически активных соединений, а также стабилизаторов свойств полимерных материалов [4]. Каталитическое аминирование спиртов осуществляется при повышенных температурах в присутствии катализаторов на основе оксидов алюминия, хрома, титана, ванадия, железа, никеля молибдена, магния, а также солей тория и природных алюмосиликатов [5].
Полифторированные спирты H(CF2CF2)nCH2OH, получаемые в промышленном масштабе взаимодействием тетрафторэтилена и метанола [6], могут рассматриваться в качестве алкилирующих агентов полиаминов, в частности, различных изомерных полиалкиленполиаминов, которые одновременно способны содержать аминогруппы различной степени замещенности.
Цель работы – каталитическое N-полифторалкилирование трис(2-аминоэтил)амина полифторированным спиртом (n = 4) в присутствии высокодисперсной монтмориллонитовой глины и исследование методами одномерной и двумерной ЯМР спектроскопии структуры синтезированного соединения.
Обсуждение результатов
Каталитическое N-полифторалкилирование трис(2-аминоэтил)амина 1Н,1Н,9Н-тригидроперфторнонан-1-олом при их мольном соотношении 1:2 приводит к получению преимущественно продукта диалкилирования:
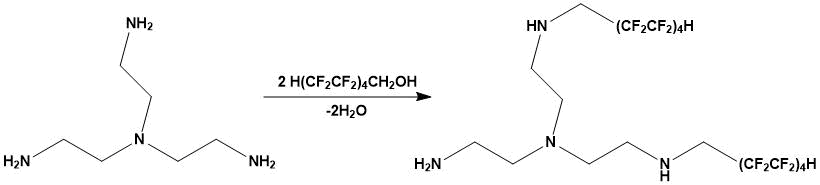
Монтмориллонитовая глина, являясь кислотой Бренстеда [7-9], способствует алкилированию трис(2-аминоэтил)амина через начальные стадии O- и N-протонирования (на схемах 1 и 2 показано только образование продукта моноалкилирования). Как видно, в обоих случаях происходит генерирование полифторированного карбокатиона, на стабильность которого оказывают существенное влияние атомы фтора, обладающие отрицательным I‑эффектом. Образование внутримолекулярной водородной связи в дизамещенном аммоний-катионе между группами CF2···H2N⊕ благоприятно сказывается на повышении его устойчивости.
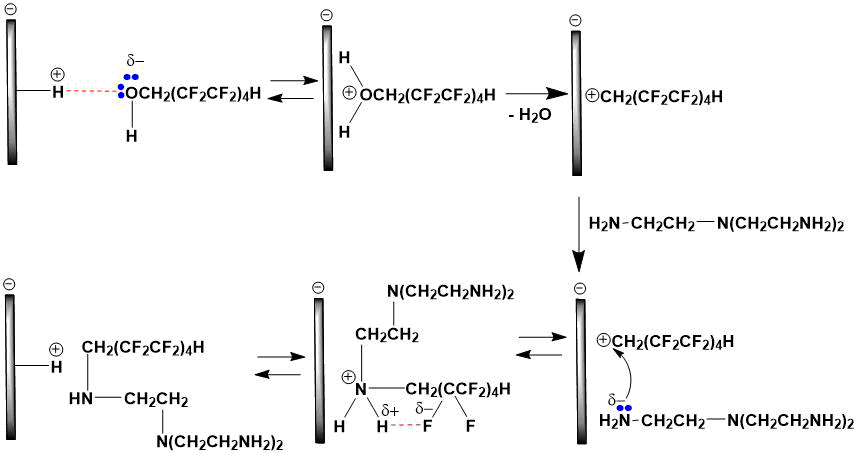
Схема 1. Механизм О-протонирования
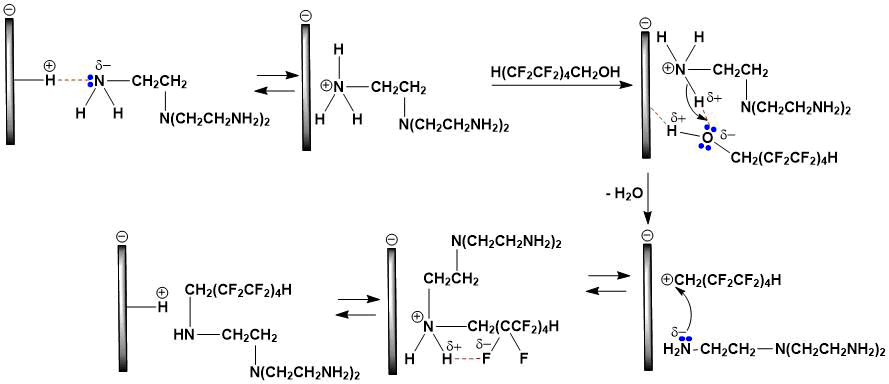
Схема 2. Механизм N-протонирования
Структурной особенностью монтмориллонитовой глины является не только бренстедовская, но и льюисовская кислотность [7-9], обусловленная наличием вакантно-орбитальных центров Мn+ (Al3+, Fe3+, Fe2+, Mn2+, Ti4+, Ca2+, Mg2+, K+, Na+). Формирование донорно-акцепторных комплексов с участием вакантных орбиталей ионов металлов может осуществляться как с неподеленными электронными парами атомов азота аминогрупп трис(2-аминоэтил)амина и кислорода гидроксильных групп 1Н,1Н,9Н-тригидроперфторнонан-1-ола (структура I), так и без участия молекул полифторированного спирта (структура II).
Таким образом, каталитическое N-полифторалкилирование трис(2-аминоэтил)амина 1Н,1Н,9Н-тригидроперфторнонан-1-олом в присутствии монтмориллонитовой глины в мольном соотношении амина и спирта 1:2 приводит к образованию дизамещенного продукта. Показан возможный вклад бренстедовских и льюисовских центров кислотности в механизм алкилирования.
Экспериментальная часть
Трис(2-аминоэтил)амин (95%, Keyingchem, Китай) очищен перегонкой и имел следующие характеристики: т.кип. 114 °С (15 мм рт. ст), d 0.976 г·мл-1, n20D 1.497. Полифторированный спирт 1Н,1Н,9Н-тригидроперфторнонан-1-ол (≥90%, ГалоПолимер, Пермь) имел т.пл. 68-70°С. Прокаленная монтмориллонитовая глина (≥98%, ТОО B–Clay, Казахстан) имела удельную поверхностью 595 м2·г-1 (по воде) и 64 м2·г-1 (по азоту), емкость катионного обмена 100 мг-экв / 100 г и была представлена в виде смеси трех основных фракций: 50-100 нм – 10 мас.%, менее 1 мкм – 80 мас.%, менее 10 мкм – 10 мас.%.
Методика синтеза. 1 мл (6.67 ммоль) трис(2-аминоэтил)амина и 5.77 г (13,3 ммоль) 1Н,1Н,9Н-тригидроперфторнонан-1-ола в присутствии каталитических количеств монтмориллонита (0.1 мг) диспергировали при частоте ультразвука 40 кГц в запаянной стеклянной ампуле при 80°С в течение 2 ч, с последующим нагревом до 120 °С в течение 6 ч. Исходные реагенты отделяли от продукта реакции экстракцией захоложенным i-PrOH при -6°С…+1°С с дальнейшей фракционной вакуумной перегонкой экстракта. Выход 2.27 г (35%), желтое масло, Rf 0.71, т. кип. 133-136 °С (15 мм рт. ст). Спектр ЯМР 1Н [CDCl3], δ, м. д.: 1.56 уш.с (2Н, H2N), 2.43-2.90 м (12Н, СН2СН2), 4.01 т (4Н, СH2CF2, J = 14.8 Гц), 6.07 т.т (2Н, HCF2, J1 = 4.8 Гц, J2 = 51.6 Гц), 7.29 c (2H, HNCH2). Спектр ЯМР 13С [CDCl3], δ, м. д.: 38.66-39.75 (CH2NH2), 41.65 (CH2CF2), 46.01 д (CH2NHCH2CF2, J = 8.1 Гц), 49.22-59.56 (NCH2CH2NH), 60.98 (NCH2CH2NH2), 104.67-114.00 (CF2). Спектр ЯМР 19F [CDCl3], δ, м. д.: -121.83 – -122.40 м (CF2), -123.70 – -129.76 м (CF2CН2), -137.21 д (CF2Н, J = 48.9 Гц). Спектр ЯМР 15N (1H-15N HMBC) [CDCl3], δ, м. д.: 18 (NH2), 30 (NH), 43 (NCH2). Найдено, %: С 29.41; Н 2.26; N 5.50. C24H22F32N4. Вычислено, %: С 29.58; Н 2.28; N 5.57. М 974.41.
Спектры ЯМР регистрировали при комнатной температуре на приборе Bruker AVANCE III HD (400 МГц) в СDCl3 (1H – 400.17 МГц, 13С – 161.99 МГц, 19F – 376 МГц), используя в качестве внутреннего стандарта тетраметилсилан. Химические сдвиги ядер 19F определены относительно CFCl3, а ядер 15N относительно жидкого аммиака, как внешнего стандарта. Элементный анализ проводили на анализаторе CHNS/O Euro EA3100. ТСХ осуществляли на пластинах Sorbfil (Россия), элюент – хлороформ–ацетон (1:1).
Список литературы
1. Yang Y., Taponard A., Vantourout J. C., Tlili A., Synthesis of Fluorinated Amines: A Personal Account, ACS Org. Inorg. Au., 2023, 3(6), 364-370.
2. Yang L., Fan W.-X., Lin E., Tan D.-H., Li Q., Wang H., Synthesis of α-CF3 and α-CF2H amines via the aminofluorination of fluorinated alkenes, Chem. Commun., 2018,54, 5907-5910.
3. Baasner B., Klauke E., Hagemann H., Amines containing fluoroalkyl groups: Methods of synthesis and properties, Journal of Fluorine Chemistry, 1983, 23(5), 478.
4. Кудашев С. В., Методы введения поли- и перфторированных фрагментов в макромолекулярные системы (Обзор), Fluorine notes, 2020, 3(130), 3-4.
5. Клюев М. Б., Хидекель М. Л., Каталитическое аминирование спиртов, альдегидов и кетонов, Успехи химии, 1980, XLIX (1), 28-53.
6. Ebnesajjad S., Fluoropolymer Additives: S. Ebnesajjad, R. A. Morgan, Elsevier, William Andrew, 2019, 304 p.
7. Физико–химические особенности природных глин, Л. Г. Гилинская, Т. Н. Григорьева, Л. И. Разворотнева, Л. Б. Трофимова, Журнал неорганической химии, 2005, 50(4), 689-698.
8. Кудашев С. В., Модификация ряда гетероцепных полимеров композициями на основе полифторированных спиртов и монтмориллонита, Автореферат диссертации…доктора химических наук (специальность 02.00.06). – ВолгГТУ, Волгоград, 2020, 48 с.
9. С. В. Кудашев, Ю. М. Шульга, Строение композиционного материала на основе полифторированного спирта и монтмориллонита, Журнал физической химии, 2018, 92(10), 1582-1587.
Статья рекомендована к публикации членом редколлегии к.х.н. В.Л. Дон
Fluorine Notes, 2024, 153, 3-4


