Поступило в редакцию: Декабрь 2023
УДК 54.057
Fluorine Notes, 2024, 152, 3-4
Способы получения фторсульфонилперфторвиниловых эфиров
О.С. Базанова, А.С. Одиноков, Е.В. Ирисова, В.Г.Барабанов
АО «Российский научный центр «Прикладная химия (ГИПХ)», г. Санкт-Петербург
Аннотация: рассмотрены основные методы получения фторсульфонилперфторвиниловых эфиров - 1,1,2,2-тетрафтор-2-[(трифторвинил)окси]этансульфонил фторида (мономера ФС‑81) и 1,1,2,2,3,3-гексафтор-3-[(трифторвинил)окси]пропансульфонил фторида (мономера ФС-101), которые являются сырьем для получения перфторированных полимерных ионообменных мембран, используемых для создания топливных элементов.
Ключевые слова: перфторвиниловые эфиры, мономеры, синтез, сополимеризация, перфторированные мембраны, топливные элементы.
Введение
Водородные топливные элементы (ТЭ) считаются будущим мировой энергетики благодаря своей эффективности и экологической безопасности. В ТЭ энергия химической реакции преобразуется в электрическую напрямую без необходимости сначала преобразовывать её в тепло или механическую работу вращения турбин. Из-за этого КПД топливных элементов существенно выше, чем в тепловых электростанциях. Кроме того, топливом здесь служит водород и кислород, а отходом является водяной пар.
Перфторированные мембраны типа Nafion разработки компании Du Pont, Aquivion фирмы Solvay Solexis Technology, Aciplex фирмы Asahi Glass Company, отечественные мембраны МФ-4СК и др. широко применяются для изготовления низкотемпературных ТЭ. Процесс получения ионообменной мембраны для ТЭ состоит из следующих стадий:
- синтез перфторвиниловых эфиров, содержащих сульфогруппу (-SO2F)
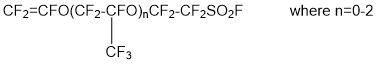
- сополимеризация синтезированного перфторвинилового эфира с тетрафторэтиленом с получением сополимера:
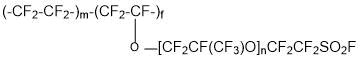
- изготовление ионообменных мембран на основе сополимера:
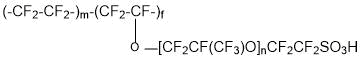
Практически единственным промышленным типом ионообменных мембран долгое время были перфторированные сульфокатионные мембраны типа Nafion. Сырьем для получения этого типа мембран является тетрафторэтилен и перфтор(3,6-диокса-4-метил-7-октен)сульфонилфторид (ФС-141). Главным преимуществом этих мембран является высокая проводимость и химическая стойкость, недостатком – низкие рабочие температуры (не более 90°С).
Мембраны типа Aquivion (сополимера тетрафторэтилена и 1,1,2,2-тетрафтор-2-[(трифторвинил)окси]этансульфонилфторида (мономер ФС-81):
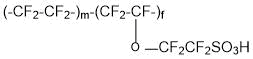
и мембраны типа Aciplex (сополимера тетрафторэтилена и 1,1,2,2,3,3-гексафтор-3-[(трифторвинил)окси]пропансульфонил фторида (мономер ФС-101):
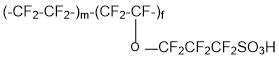
работоспособны при температуре 130°С и выше. Замена мембран Nafion на перфторированные Aquivion и Aciplex позволяет исключить вероятность отравления Pt катализатора в каталитических слоях ТЭ за счет изменения равновесия сорбции окиси углерода (СО) и водорода на Pt.
Создание производства ионообменных мембран в РФ возможно только после создания производства подходящих фторсодержащих сульфомономеров (перфторвиниловых эфиров). Технология получения ФС-141 (мономера для получения мембраны типа Nafion), которая является наиболее сложной стадией синтеза ионообменных мембран, в РФ разработана [1]:
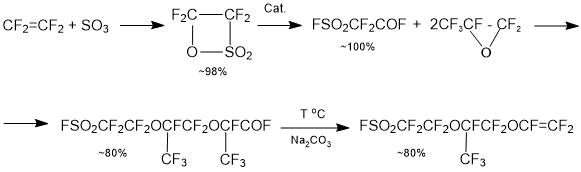
Технологии получения фторсульфонилперфторвиниловых эфиров ФС-81 и ФС-101 для мембран типа Aquivion и Aciplex находятся в стадии исследований, поэтому выбор оптимального синтеза является актуальной задачей.
В настоящее время большая часть известных в научно-технической литературе исследований, направленных на разработку способов получения перфторвиниловых эфиров (в том числе, мономеров ФС-81 и ФС-101), основана на применении трех основных методов (или их сочетаний):
Метод 1. Процессы, основанные на реакциях перфторацилфторидов с окисью гексафторпропилена (ОГФП) в присутствии катализаторов (KF, CsF) с последующим разложением продуктов присоединения (гидролиз, пиролиз) [1-4];
Метод 2. Процессы, основанные на дехлорировании цинком аддуктов 1,2-дифтор-1,2-дихлорэтилена с перфторгипофторитами, которые получают каталитическим фторированием перфторацилфторидов элементным фтором [5-10];
Метод 3. Процессы, основанные на реакциях галогенирования и дегалогенирования субстратов различной природы [4, 11, 12].
Для всех трех методов проблемным может быть синтез труднодоступных исходных веществ и необходимость использования опасных в обращении реагентов. Несмотря на интенсивно ведущиеся исследования, до сих пор для перфторвиниловых эфиров не разработано высокоэффективных методов синтеза, которые позволили бы получать их по простым технологическим схемам с высоким выходом и низкой стоимостью.
Целью настоящего исследования является рассмотреть возможные перспективные методы синтеза перфтормономеров ФС-81 и ФС-101.
Способы получения мономера ФС-81
Метод 1.1. «Стандартный» способ, основанный на присоединении к фторсульфонилдифторацетилфториду одной молекулы ОГФП с последующим пиролизом продукта присоединения по схеме (1) для синтеза мономера ФС-81 не может быть использован ввиду того что, вместо целевого продукта, он ведет к получению циклического сультона (I) [13, 14]:
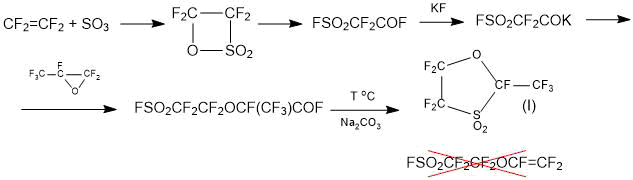
Схема 1.
Для синтеза мономера ФС-81 разработаны модифицированные варианты схемы (1).
Вариант 1: Мономер ФС-81 может быть получен, если заменить ОГФП на хлорпентафторпропиленоксид, схема (2) [15]:
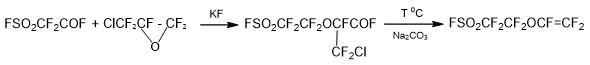
Схема 2.
Основной недостаток метода – малая доступность хлорпентафторпропиленоксида и невозможность его синтеза с высоким выходом. По этой причине схема (2) не может рассматриваться как эффективный способ получения мономера ФС-81 с низкой стоимостью.
Вариант 2: Получение мономера ФС-81 по схеме (3) [16, 17]:
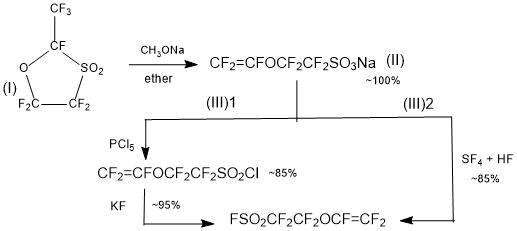
Схема 3.
Показано [16], что при взаимодействии сульфона (I) с эквимолекулярным количеством алкоголята щелочного
металла в инертном растворителе происходит раскрытие цикла и, с практически количественным выходом,
образуется сульфонат натрия перфторвинилового эфира (II). Последний по схемам 3(1) [16] или 3(2)
[17] может быть превращен в мономер ФС-81.
Метод 1.2. Фирмой Solvay Solexis предложен способ получения мономера ФС-81, основанный на взаимодействии перфтор-2-фторсульфонилэтилгипофторита (I) с 1,2-дифтор-1,2-дихлорэтиленом при низкой температуре с последующим дегалогенированием образовавшегося аддукта по схеме (4):
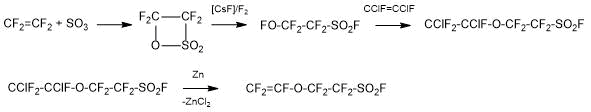
Схема 4.
Патентом фирмы Ausimont [6] защищен одностадийный процесс получения гипофторита (I), основанный на непрерывном пропускании перфтор-β-сультона (II) в смеси фтора и инертного газа (азот) над фторированным катализатором (CsF, KF), который был либо фиксирован на подложке с хорошим теплообменом (медь или ее сплавы), либо суспендирован в жидкой среде или инертном растворителе, при непрерывном удалении продуктов реакции из газовой фазы. Конверсия и чистота гипофторита близки к 100%. Процесс исключает необходимость проведения стадии изомеризации перфтор-β-сультона (II) в фторсульфонилперфторацетилфторид.
Метод 1.3. Фирмой Daikin предложен способ получения мономера ФС-81 по схеме (5) [12]:
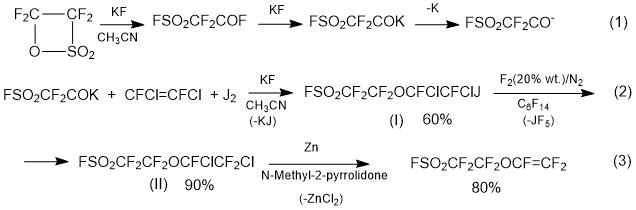
Схема 5.
На стадии 1 взаимодействием перфторалкоксида фторсульфонилацетилфторида (фторангидридный изомер тетрафторэтан-β-сультона) с 1,2-дифтор-1,2-дихлорэтиленом и иодом (катализатор – KF, CsF) получают иодзамещенный эфир (I) (1,1,2,2-тетрафтор-2-[(3,4-дифтор, 3,4-дихлор, 4-иодэтан)окси]этансульфонилфторид) (I); выход 60%.
На стадии 2 путем обработки иодпроизводного (I) газовой смесью F2/N2 проводят обменную реакцию J/F и получают Cl,F-замещенный эфир (II) (1,1,2,2-тетрафтор-2-[(3,4,4-трифтор, 3,4-дихлорэтан)окси]этансульфонил-фторид); выход ~90%.
На стадии 3 дехлорируют Cl,F-замещенный эфир (II) цинком в органическом растворителе (N-метилпирролидон) и получают перфторвиниловый эфир (III) (мономер ФС‑81); выход ~80%.
Предложенная схема обеспечивает возможность синтеза перфторвинилового эфира с достаточно высоким выходом и может рассматриваться как перспективный метод получения мономера ФС-81.
Способы получения мономера ФС-101
Метод 2.1. Показано [18], что при электрохимическом фторировании 1,3‑пропансультона и 1,4-бутансультона в жидком HF с достаточно высоким выходом происходит раскрытие циклов и изомеризация сультонов в перфтор-3-фторсульфонилпропионилфторид формулы FSO2CF2CF2COF и в перфтор-4-фторсульфонилбутаноилфторид формулы FSO2CF2CF2CF2COF, соответственно.
Это дает возможность использовать для получения мономера ФС-101 простой «стандартный» способ, основанный на присоединении к перфтор-3-фторсульфонил-пропионилфториду одной молекулы ОГФП с последующим пиролизом продукта присоединения по схеме (6):
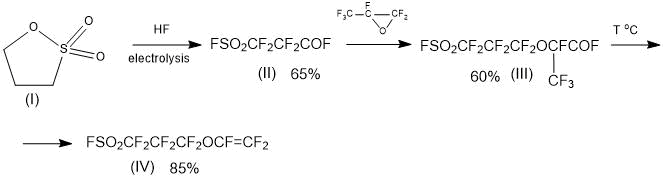
Схема 6.
Предложенная схема (6) может рассматриваться как перспективный способ получения мономера ФС-101.
Метод 2.2. Способ получения мономера ФС-101, основанный на «традиционных» методах синтеза, разработан фирмой Asahi Glass 40 лет тому назад [4, 18, 19] и до настоящего времени с незначительными видоизменениями остается практически значимым способом его синтеза по следующей общей схеме (7) [4]:
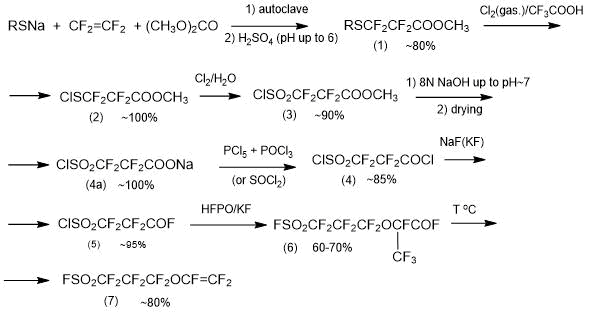
Схема 7.
На первой стадии путем взаимодействия тетрафторэтилена с эфиром карбоновой кислоты (предпочтительно, с диметилкарбонатом) и меркаптидом формулы RSM (R – алкил (Me, Et, Bu, Am), M – щелочной металл (Na, K)) в инертном растворителе (тетрагидрофуран, эфир и т.п.) получают эфир формулы RSCF2 CF2COOCH3 с выходом ~80%. Тетрафторэтилен используют в газообразном состоянии. Он может вводиться в реакционную систему под любым давлением – пониженным (предпочтительно) или повышенным. Процесс проводится до тех пор, пока в условиях реакции давление тетрафторэтилена не станет постоянным. Допустимый температурный интервал – 0 – 80 °C. Реакцию, по возможности, ведут при пониженной температуре, чтобы предотвратить образование кетона формулы (RSCF2CF2)2CO (побочный продукт синтеза).
Все полупродукты и целевой продукт синтеза получают с высоким выходом, что позволяет, несмотря на многостадийность процесса, рассматривать возможность его успешного использования для препаративного получения мономера ФС-101.
Заключение
На основании литературных данных наиболее перспективными методами получения фторсульфонилперфторвиниловых эфиров являются:
- для мономера ФС-81 формулы FSO2CF2CF2OCF=CF2 метод 1.1 (вариант 2), позволяющий получить мономер ФС-81 с выходом не менее 85%;
- для мономера ФС-101 формулы FSO2CF2CF2CF2OCF=CF2 метод 2.1, позволяющий получить мономер ФС-101 с выходом не менее 80%.
Предложенные методы могут быть использованы для разработки на их основе крупномасштабных способов производства мономеров ФС-81 и ФС-101.
Список литературы
- Фторсодержащие мембранно-каталитические полимерные материалы и системы (Сборник научных трудов) // Под ред. Барабанова В.Г., Корнилова В.В., Максимова Б.Н., Санкт-Петербург, 2010, Изд. Серебряный век, 124 с, ISBN 978-5-902238-70-6.
- Arcella V., Ghielmi A., Tommasi G., Ann. N. Y. Acad. Sci., 2003, 984, 226-44.
- Process for producing fluorinated vinyl ether, US 7196235 B2, 2007.
- Fluorierte vinylaetherverbindungen, ihre herstellung und verwendung, DE 3047439 A1, 1981.
- Способ получения хлорфторалкиловых эфиров, SU 1533624 A3, 1989.
- Process for preparing Hypofluorites and bis-hypofluorites, EP 0259817 A2, 1987.
- Method and image processing system for reconstruction of an image, EP 0269993 A2, 1991 (см. также Cпособ получения 2-бром-перфторэтилгипофторита, SU 1784040 A3, 1992).
- Process for the preparation of fluorooxy-fluorosulfonyl compounds by direct fluorination of fluoro-beta-sultones, EP 0384261 A1, 1990.
- Фторированные производные бисвинилоксиметана (варианты), полимеры и сополимеры на их основе, RU 2144044 C1, 1995.
- Process for the production of ethers, typically thf, US 6936727 B2, 2005.
- Production of perfluoro(alkyl vinyl ethers), US 5350497 A, 1994.
- Pat. US5616813, Vinyl ether compound, process for producing the same and copolymer containing the same, 1997
- 1) Sulphonic acid derivatives of fluorocarbon vinyl ethers, and polymers thereof, GB 1034197 A, 1966; 2) Novel Fluorinated Compounds, GB 2053902 A, 1980.
- Fluorocarbon ethers containing sulfonyl groups, US 3301893 A, 1967.
- Trichlorotrifluoropropylene oxide and process for producing the same, Pat. JP4666107, 2011
- Preparation of sulfoncacid containing fluorocarbon vinyl ethers, US 3560568A, 1971.
- Process for producing fluorinated fluorosulfonylalkyl vinil ether, US 7005545 B2, 2006.
- Process for the preparation of (omega-fluorosulfonyl) haloaliphatic carboxylic acid fluorides, EP 0062430 A1, 1982.
- Fluorinated copolymers and cation exchange membrane and process for producing the same, GB 2051831 A, 1981.
Статья рекомендована к публикации членом редколлегии к.х.н. М.А. Манаенковой
Fluorine Notes, 2024, 152, 3-4


