Поступило в редакцию: Апрель 2022
УДК 541.64 :547.621.81:547.655
Fluorine Notes, 2022, 141, 5-6
ВЛИЯНИЕ 2,3-БИС(ПОЛИФТОРАЛКОКСИ)-[1,4]-НАФТОХИНОНОВ И 2-ХЛОР-3-(2-ПРОПЕНОКСИ)-1,4-НАФТОХИНОНА НА ТЕРМОСТОЙКОСТЬ ПОЛИМЕТИЛМЕТАКРИЛАТА
О. А. Мельник, М. И. Бузин, В. И. Дяченко
Институт элементоорганических соединений им. А. Н. Несмеянова РАН, Российская Федерация, 119991, г. Москва, ул. Вавилова, 28
e-mail: omel@ineos.ac.ru
Аннотация: Синтезированы сополимеры метилметакрилата с 2-хлор-3-(2-пропенокси)-1,4-нафтохиноном и полимеры с добавками 2,3-бис(полифторалкокси-[1,4]-нафтохинонов. Изучены их физико-химические свойства и термические характеристики. Установлено, что использование в качестве добавки 2,3-дизамещенных фторсодержащих [1,4]-нафтохинонов приводит к повышению термоокислительной устойчивости полиметилметакрилата.
Ключевые слова: 2-хлор-3-(2-пропенокси)-1,4-нафтохинон, 2,3-бис(полифторалкокси)-[1,4]-нафтохиноны, полиметилметакрилат, свободно-радикальная (cо)полимеризация, термостойкость.
Акриловые полимеры, характеризующиеся высокой прозрачностью, хорошей растворимостью, нашли широкое практическое применение для создания различных материалов. Полиметилметакрилат (ПММА) – прозрачный полимер с хорошими оптическими, механическими и электроизоляционными свойствами, высокой атмосферостойкостью, используется в качестве конструкционного материала в авиа-, автомобиле-, приборо- и судостроении, медицине, оптике, светотехнике [1, 2]. Для снижения деструктивных процессов при повышенных температурах в полимер вводят стабилизаторы, различные модифицирующие добавки, а также антиоксиданты [1].
Ранее мы показали стабилизирующее действие на термоокислительную устойчивость ПММА 2-хлор-3-полифторалкокси-[1,4]-нафтохинонов, имеющих различную длину полифторалкоксильного радикала [3]. Известно, что для модификации полимеров часто используют и метод сополимеризации с целью повышения их функциональных, в том числе термических, характеристик [4]. В настоящей работе свободно-радикальной сополимеризацией в блоке синтезированы сополимеры метилметакрилата (ММА) и 2-хлор-3-(2-пропенокси)-1,4-нафтохинона разного состава и определена их термостойкость.
Впервые 2-хлор-3-(2-пропенокси)-1,4-нафтохинон (III) был получен реакцией 2,3‑дихлор-1,4-нафтохинона (I) с аллиловым спиртом (II) в тетрагидрофуране в присутствии К2СО3 на протяжении 3 часов [5]. После удаления в вакууме растворителя и последующей хроматографии остатка на силикагеле выход соединения III составил 78%.
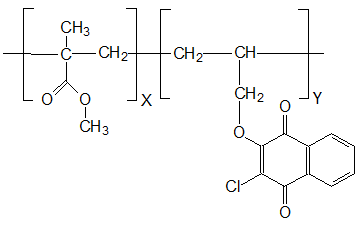
Схема 1.
Нам удалось упростить условия проведения реакции и процедуру выделения конечного продукта, существенно увеличив его выход. Оказалось, что при проведении реакции в аллиловом спирте в присутствии эквимольного количества поташа соединение III образуется в течение 1,5 часов с количественным выходом. При этом значительно упрощается процедура его выделения, заключающаяся в разбавлении реакционной массы водой и фильтровании выпавшего в осадок продукта реакции. После промывания его дистиллированной водой и сушки на стеклянном фильтре получается спектрально чистый 2‑хлор-3-(2-пропенокси)-1,4-нафтохинон (III).
Свободно-радикальную сополимеризацию ММА и соединения III (1-3 мол.%) проводили в вакуумированных, запаянных стеклянных ампулах в присутствии 0,5 масс.% инициатора – динитрила азобисизомасляной кислоты (ДАК) при 60С. Сополимеры представляют собой твердые прозрачные стеклообразные образцы желтого цвета, их строение устанавливали по данным ИК-спектроскопии и элементного анализа (Рис. 1).

Рисунок 1. Структурная формула сополимеров ММА и 2-хлор-3-(2-пропенокси)-1,4-нафтохинона.
Они растворимы в бензоле, толуоле, хлорированных углеводородах и не растворимы в гексане, серном эфире, низших спиртах и воде.
После исследования основных физико-химических характеристик полученных сополимеров представлялось целесообразным изучить возможность применения 2,3‑бис(полифторалкокси)-[1,4]-нафтохинонов (Рис. 2) в качестве антиоксидантных добавок при полимеризации ММА. Ранее методом циклической вольтамперометрии было показано, что эти соединения, как и 2-хлор-3-полифторалкокси-[1,4]-нафтохиноны, в апротонной среде легко подвергаются поэтапному обратимому электровосстановлению (потенциал восстановления Ео1=-0,35 В) [6]. То есть они могут замедлять термоокислительную деструкцию полимеров за счет нейтрализации образующихся радикалов.
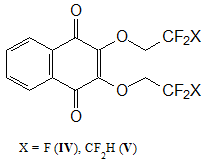
Рисунок 2. Структурные формулы 2,3-бис(полифторалкокси)-[1,4]-нафтохинонов.
Эти соединения представляют собой легкоплавкие, стабильные, хорошо растворимые в органических растворителях вещества. Они могут быть получены взаимодействием коммерчески доступных 2,3-дихлор-[1,4]-нафтохинона и фторсодержащих спиртов, производимых в промышленных масштабах [7]. Свободно-радикальной полимеризацией ММА в массе были синтезированы образцы ПММА с добавками соединений IV, V и изучена их термоокислительная устойчивость.
Термостойкость полученных (со)полимеров оценивали по температуре начала разложения Тд, за которую принимали температуру, при которой потеря массы анализируемого образца составляла 10% от изначальной. Ее определяли методом динамического термогравиметрического анализа при скорости нагревания 10C/мин на воздухе. Результаты приведены в Таблице 1.
Сравнение полученных результатов с данными термогравиметрического анализа ПММА свидетельствует о понижении термоокислительной стабильности сополимеров ММА и 2-хлор-3-(2-пропенокси)-1,4-нафтохинона (образцы 3 и 3’). Так, Тд сополимера ММА и соединения III молярного состава 99:1 равна Тд ПММА (265С). С увеличением содержания мономера III до 3 мол.% Тд составляет 208С. Это может быть связано с тем, что при сополимеризации аллильного соединения III происходит передача цепи на мономер, что приводит к уменьшению молекулярного веса и понижению Тд [8, 9].
Таблица 1. Термостойкость (со)полимеров ММА с добавками 2,3-замещенных [1,4]-нафтохинонов общей формулы:
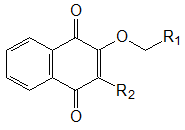
|
№ образца |
R1 |
R2 |
Тд, °C |
|
|
99:1 |
97:3 |
|||
|
ПММА* |
– |
– |
265 |
|
|
1, 1’* |
CF3 |
Cl |
305 |
320 |
|
2, 2’* |
CF2CF2H |
Cl |
306 |
315 |
|
3, 3’ |
CH=CH2 |
Cl |
265 |
208 |
|
4, 4’ |
CF3 |
OCH2CF3 |
320 |
302 |
|
5, 5’ |
CF2CF2H |
OCH2C2F4H |
320 |
304 |
* данные работы [3]
Найдено, что Тд композитов ПММА с добавками 1 мол.% 2,3-бис(полифторалкокси)-[1,4]-нафтохинонов IV, V равна 320°C и её величина не зависит от длины полифторалкильного заместителя (образцы 4 и 5). Такое же значение Тд имел полимер ММА с добавкой 3 мол.% 2-хлор-3-(2,2,2-трифторэтокси)-[1,4]-нафтохинона (образец 1’).
Экспериментальная часть
Спектры ЯМР 1Н и 19F записаны в СDCl3 на приборе Bruker Avance 400 (400 и 376 МГц соответственно). Химические сдвиги 1Н приведены относительно Me4Si (внутренний стандарт), 19F относительно CF3CO2H (соединение IV) и СFCl3 (соединение V) - внешний стандарт. ИК-спектры сняты на Фурье-спектрометре Bruker Vertex 70 v с разрешением 4 см-1 в режиме нарушенного полного внутреннего отражения, используя приставку PIKE Glady ATR c алмазным рабочим элементом. Динамический термогравиметрический анализ проведен на дериватографе Q-1500 фирмы МОМ.
В качестве исходных реагентов использовали 2,3-дихлор-[1,4]-нафтохинон, 98% [САS 117-80-6] и аллиловый спирт, 99,5% [САS 107-18-6] фирмы ABCR. MMA (Aldrich, 99%) перегоняли при пониженном давлении. ДАК (Aldrich, 98%) очищали перекристаллизацией из метанола.
2-Хлор-3-(2-пропенокси)-1,4-нафтохинон (III)
В стеклянную коническую колбу, снабженную магнитной мешалкой и обратным холодильником с хлоркальциевой трубкой, помещали 227 мг (1 ммоль) 2,3-дихлор-[1,4]-нафтохинона, 1,5 г аллилового спирта и 138 мг (1ммоль) безводного поташа. Реакцию вели при перемешивании и комнатной температуре на протяжении 1.5 часов. ТСХ-контроль реакции осуществляли в системе хлороформ-циклогексан = 2:3. При интенсивном перемешивании в реакционную массу прибавляли по каплям 5 мл дистиллированной воды. Образовавшийся при этом желтый осадок отфильтровывали, промывали водой и сушили на фильтре до постоянного веса. Получали 235 мг светло-желтого аморфного соединения. Выход 98,7%, т. пл. 75-76оС. Найдено, %: С, 62,58; Н, 3,71; Cl, 14,31. C13H9ClO3. Вычислено, %: С, 62,70; Н, 3,65; Cl, 14,24. Спектр ЯМР 1Н (400 МГц, СDСl3, δ, м.д., J/Гц): 5.10 (уш.с, 2H, OCH2), 5.31 (уш.д, 1H, CH=CH2, 3J = 10.8 Гц), 5.45 (уш.д, 1H, CH=CH2, 3J = 17.4 Гц), 6.02–6.10 (м, 1H, CH=CH2), 7.75 (уш.с, 2H, Ar), 8.08 (уш.д, 1H, Ar, 3J = 7.8 Гц), 8.14 (уш.д, 1H, Ar, 3J = 7.8 Гц).
2,3-Бис(полифторалкокси)-[1,4]-нафтохиноны синтезировали по методике, описанной в работе [7].
2,3-Бис-(2,2,2-трифторэтокси)-[1,4]-нафтохинон (IV)
Т. пл. 81-82оС. Найдено, %: С, 47,58; Н, 2,24; F, 31,88. C14H8F6O4. Вычислено, %: С, 47,47; Н, 2,28; F, 32,18. Спектр ЯМР 1Н (СDСl3, δ, м.д., J/Гц): 8,10 (д.кв, 2Н, Аr); 7,78 (д.кв, 2H, Ar), ABCD-cистема; 4,78 (кв, 4Н, 2 OCH2, 2J=8). Спектр ЯМР 19F (СDСl3, δ, м.д., J/Гц): 2,77 (c, 3F, CF3).
2,3-Бис-(2,2,3,3-тетрафторпропокси)-[1,4]-нафтохинон (V)
Т. пл. 42-43оС. Найдено, %: С, 45,78; Н, 2,25; F, 36,02. C16H10F8O4. Вычислено, %: С, 45.95; Н, 2,41; F, 36,34. Спектр ЯМР 1Н (СDСl3, δ, м.д., J/Гц): 8,09 (д.кв, 2 Н, Аr); 7,79 (д.кв, 2H, Ar), ABCD-cистема; 6,15 (тт, 2Н, 2 CF2H, 2JH-F=64, 3JH-F = 4); 4,78 (т, 4 Н, ОСН2, 2JH-F =16). Спектр ЯМР 19F (СDСl3, δ, м.д., J/Гц): -125,40 (c, 2 F, CF2); -138,86 (c, 2 F, CF2).
Получение сополимера ММА и 2-хлор-3-(2-пропенокси)-1,4-нафтохинона (III) при мольном соотношении звеньев 99:1
К смеси 2,640 г свежеперегнанного ММА и 0,066 г (III) прибавляли 0,014 г (0,5 масс.%) ДАК в качестве инициатора сополимеризации. Реакционную смесь фильтровали в стеклянную ампулу и освобождали от воздуха трёхкратным повторением циклов замораживание - размораживание в вакууме. После этого ампулу запаивали и помещали в термостат, нагретый до 60 С. Через 6 ч ампулу вынимали, охлаждали и вскрывали. Прозрачный твердый сополимер желтого цвета сушили в вакууме при 40С в течение 24 ч до постоянного веса. Найдено, %: С, 60,29; Н, 7,88. Вычислено, %: С, 60,12; Н, 7,97. В ИК-спектре сополимера содержатся полосы поглощения, характерные для звеньев как ММА, так и соединения III : 1674, 1590, 1568 см-1 (фрагменты [1,4]-нафтохинона); 1721 см-1 (С=О ММА). Отсутствуют полосы поглощения валентных колебаний связей С=С при 1622 и 1640 см-1, имевшиеся в ИК-спектрах исходных мономеров.
Аналогично были синтезированы сополимеры ММА и соединения III при мольном соотношении звеньев 97:3.
Получение ПММА с 2,3-бис-(2,2,2-трифторэтокси)-[1,4]-нафтохиноном (IV) при мольном соотношении 99:1
К раствору 2,473 г свежеперегнанного метилметакрилата и 0,089 г (IV) прибавляли 0,013 г (0,5 масс.%) ДАК в качестве инициатора полимеризации. Приготовленную реакционную массу фильтровали в стеклянную ампулу, которую затем дегазировали путем трехкратного замораживания погружением в жидкий азот с последующим размораживанием в вакууме, запаивали и помещали в термостат. Температура полимеризации 60С. Через 6 ч ампулу вынимали, охлаждали и вскрывали. Прозрачный твердый полимер желтого цвета сушили в вакууме при 40С в течение 24 ч до постоянного веса.
Получение ПММА с 2,3-бис-(2,2,3,3-тетрафторпропокси)-[1,4]-нафтохиноном (V) при мольном соотношении 99:1
Получали аналогично вышеописанному способу из 2,425 г свежеперегнанного ММА и 0,313 г соединения V.
Таким же методом были синтезированы образцы ПММА с соединениями IV, V при мольном соотношении 97:3.
Выводы
Таким образом, установлена взаимосвязь между строением полученных 2,3‑дизамещенных [1,4]-нафтохинонов и возможностью их применения в качестве антиоксидантных добавок при полимеризации ММА. Показано, что использование 1 мол.% 2,3-бис(полифторалкокси)-[1,4]-нафтохинонов IV, V приводит к повышению термоокислительной устойчивости ПММА на 55С.
Благодарности
Работа выполнена при поддержке Министерства науки и высшего образования Российской Федерации с использованием научного оборудования Центра исследования строения молекул ИНЭОС РАН.
Список литературы
- Технические свойства полимерных материалов, под ред. В.К. Крыжановского, 2-ое изд. СПб.:Профессия, 2005, 235 с.
- В. Дебский. Полиметилметакрилат. М.: Химия, 1972, 152 с.
- O.A. Melnik, M.I. Buzin, V.I. Dyachenko, Fluorine notes, 2021, 138(5), 1-2.
- В.В. Киреев. Высокомолекулярные соединения. М.: Высшая школа, 1992, 512 с.
- M. Kadela-Tomanek, E. Bebenek, E. Chrobak, M. Latocha, S. Boryczka, Molecules, 2017, 22, 447.
- S.M. Peregudova, V.I. Dyachenko, Fluorine notes, 2021, 135(2), 7-8.
- V.I. Dyachenko, Fluorine notes, 2021, 134(1), 5-6.
- G. Moad, D. H. Solomon.The сhemistry of radical polymerization, 2nd ed. Amsterdam, Elsevier, 2006, p. 296.
- A. Matsumoto, T. Kumagai, H. Aota, H. Kawasaki, R. Arakawa, Polymer Journal, 2009, 41(1), 26–33.
Статья рекомендована к публикации членом редколлегии к.х.н. М.А. Манаенковой
Fluorine Notes, 2022, 141, 5-6


