Поступило в редакцию: Январь 2022
УДК 543.51+547
Fluorine Notes, 2022, 140, 5-6
ПОСЛЕДОВАТЕЛЬНОСТИ ФРАГМЕНТАЦИЙ - ИОННЫЕ СЕРИИ МАСС-СПЕКТРОВ н-АЛКИЛГАЛГЕНИДОВ, α,ω-ДИГАЛОГЕНАЛКАНОВ, α,ω-ДИГАЛОГЕНПЕРФТОРАЛКАНОВ.
ЭФФЕКТ МАССЫ ТЕРМИНАЛЬНОГО ГАЛОГЕНИДА И МОЛЕКУЛЯРНОЙ МАССЫ ЦЕПИ
Н.Д. Каграманов
Институт элементоорганических соединений им. А. Н. Несмеянова Российской академии наук, 119991, ГСП-1, Москва, В-334, ул. Вавилова, д. 28
e-mail: ndkagram@gmail.com
Аннотация: В масс-спектрах эйкозана C20H42, 1-бром эйкозана
и 1,20-дибром эйкозана (из библиотек NIST) установлены последовательности распада - шесть и соответственно
восемь ионных серий. Масс-спектры α,ω-дихлор, -дибром и -дииод перфторалканов включают четыре ионных
серии. При увеличении молекулярной массы гомологов н-алкилгалогенидов и α,ω-дигалогеналканов снижение
интенсивностей пиков +C4H8Hal и +C5H10Hal
– результат уменьшения стабилизирующего влияния массы атома галогенида, распределяющегося на всю
цепь от +.M до +C4H8Hal.
Терминальные атомы галогенидов в алкильных и перфторалкильных цепях стабилизируют серии ионов от
M+. до фрагментных ионов, пики которых имеют максимальные
интенсивности и минимальные массы. Минимальные стабилизируемые галогенидами массы фрагментов имеют
близкие значения: 56 и 70 Да (C4H8 , C5H10 ) в
алкильных и 50 и 100 Да (CF2, C2F4) в перфторалкильных цепях. На
примерах масс-спектров α,ω-дигалогенбутанов и α,ω-дигалогенперфторбутанов подтверждено, что интенсивность
пика иона, образующегося при отрыве терминального галогенида прямо пропорциональна массе отрываемого
галогенида и обратно пропорциональна массе алкильной или перфторалкильной цепи. В сериях постепенно
возрастающих пиков фрагментных ионов масс-спектров н-алканов и циклоалканов, все предпоследние пики
имеют максимальные интенсивности, как по причине оптимальных соотношений масс и энергий, так и возрастающей
возможности циклизации или перегруппировки. С уменьшением длины цепи вероятность циклизации или перегруппировки
линейного иона увеличивается. Для графической оценки перераспределений энергий ионов и нейтральных
молекул этилена, происходящих в ходе фрагментации, предложен метод фиктивных интенсивностей этилена.
В значительном интервале масс, график интенсивностей этилена, его симметричный и последовательный
рост, зеркально повторяет график интенсивностей алкильных ионов. С ростом интенсивностей пиков алкильных
ионов соответствующие интенсивности этилена, а также их полярность изменяются не симбатно, что дает
дополнительную информацию, об образовании и завершающих распадах перегруппировочных ионов. Графики
фиктивных интенсивностей отрывов этилена, в масс-спектрах эйкозана и 1-бром пентакозана позволяют
заключить, что базовый алкильный ион +C4H9 m/z 57- является перегруппировочным
третичным ионом +C(CH3)3, который при завершающем отрыве этилена
снова перегруппировывается в линейный. Ключевые слова: ионные серии спектров, н-алканы и н-алкилгалогениды, регулярные фрагментные
группы (C2H4)n, (CF2)n, эффект массы отрываемого
радикала и массы цепи, последовательный рост интенсивностей пиков, интенсивные пики, завершающие
фрагментацию, метод фиктивных интенсивностей этилена. О первичных отрывах, алгоритмах фрагментаций и последующих процессах, происходящих
в масс-спектрах н-алканов, н-перфторалканов, н-карбоновых кислот, циклоалканов, перфторполициклоалканов
ранее сообщалось в работах [2-4]. В статье [1], посвященной влиянию на фрагментацию алкилгалогенидов и α,ω- дигалогеналканов массы отрываемого
радикала и молекулярной массы гомологов, анализ спектров был выполнен без рассмотрения и учета их
ионных серий. Это не позволило нам сделать более обоснованные выводы относительно причин снижения
интенсивностей пиков галогенсодержащих ионов при увеличении молекулярной массы гомологов, а также
объяснить влияние массы отрываемого галогенида и массы цепи на интенсивность пика образующегося иона.
В настоящем сообщении, на примерах гомологов С20 подробно рассмотрены все ионные серии фрагментации
эйкозана, 1-бром эйкозана, 1,20-дибром эйкозана. Образцы C4-C10 α,ω-дибромперфторалканов, спектры которых отсутствуют в библиотеках
NIST, предоставлены OOО НПО “ПиМ-Инвест”. Их масс-спектры ионизации электронами регистрировались
на хроматомасс-спектрометре Finnigan Polaris Q в диапазоне масс 30-700 Да, при энергии 70 эВ (капиллярная
колонка Rtx-5MS 5% дифенил / 95% диметилполисилоксан 30м, 0.25 мм внутренний диаметр, максим. Темп.
350C). Ионные серии эйкозана, 1-бром нонана, 1-бром эйкозана, 1-бром пентакозана, 1,20-дибром эйкозана Спектр эйкозана, С20H42 MW 2820 NIST#: 341441 ID#: 25337 DB: mainlib включает шесть
серий ионов. Порядок отрывов, в виде шести фрагментационных последовательностей представлен на (Рис.
1). Первичные и последующие отрывы, происходящие в шести сериях, завершаются образованием шести наиболее
интенсивных пиков ионов (m/z 57, 71, 41, 55, 56 и 70) (Рис. 1). Рисунок 1. Шесть серий ионов масс-спектра эйкозана C20H42 MW: 282 NIST#: 341441 Из шести ионных серий эйкозана C20H42 наиболее интенсивны две главных алкильных
серии пиков, возникающих при отрывах метильного и этильного радикалов и последующих выбросов этилена.
Их самыми интенсивными пиками являются: базовый пик +C4H9 с m/z
57 (кратный этиленовой и этильной группе), а также пик +C5H11 с
m/z 71 (77%) (кратный двум этиленовым группам и метильной группе). Две менее интенсивных серии алкенильных
пиков возникают в результате отрыва двух атомов водорода от одной из терминальных групп C2H5 M+. с образованием стабилизирующей винильной группы. Отрыв метильного и этильного радикалов
от противоположной терминальной группы C2H5 и последующие выбросы этилена приводят
к двум алкенильным сериям, завершающимся пиками средней интенсивности +C3H5 c
m/z 41 (31%) и +C4H7 с m/z 55 (27%). Две наименее интенсивных серии
олефиновые пиков образуются при отрыве атома водорода от одной из терминальных групп CH3 M+., отрыве метильного (этильного) радикала от противоположной терминальной группы C2H5 и последующих выбросов этилена. Самыми интенсивными пиками олефиновых серий являются: пик +C4H8 с
m/z 56 (15%) (кратный двум этиленовым группам) и пик +C5H10 с m/z
70 (13%) (кратный этиленовой и пропиленовой группам). Спектр 1-бром эйкозана C20H41Br
MW: 360 NIST#: 232983 ID#: 24229 DB: mainlib (Рис. 2) включает восемь серий ионов. Шесть алкильных
серий, приводящих к интенсивным пикам с m/z 57, 43, 55, 41, 56 и 70 a.e.м. (графики синего цвета)
и две бромалкильных серии с интенсивными пиками m/z 135 и 149 (графики красного цвета). Рисунок 2. Восемь серий ионов масс-спектра 1-бром эйкозана C20H41Br MW: 360 Две наиболее интенсивных серии алкильных ионов, завершающихся пиками с (m/z 57 и 43) и две серии бромалкильных
ионов, завершающихся пиками с (m/z 135 и 149) результат двух параллельных фрагментаций, алкильной
и бромалкильной, начинающихся c противоположных терминальных групп молекулярного катион радикала.
Остальные четыре серии пиков: две алкенильных (m/z 55 и 41) и две олефиновых (m/z 56 и 70) образуются
в двух сопутствующих процессах алкильной фрагментации в результате фрагментации обоих терминальных
групп молекулярного катион радикала. Когда до наиболее интенсивного пика серии число метиленовых
групп нечетное, как в случае алкильной серии с пиком m/z 43 или в олефиновой серии с пиком m/z 70,
то в этих сериях сначала происходит один отрыв пропилена – C3H6, а затем последовательные
выбросы этилена. Спектр 1-бром нонана C9H19Br MW: 206 NIST#: 9449 ID#: 120721
DB: mainlib (Рис. 3) включает восемь серий ионов. Каждая из восьми серий завершается пиком, имеющим
в данной серии максимальную интенсивность (m/z 43, 57, 41, 55, 56, 42, 135 и 149). Две олефиновых
серии ионов завершаются пиками с m/z 42 и 56. Рисунок 3. Восемь серий ионов масс-спектра 1-бром нонана C9H19Br MW: 206 Спектр 1-бром пентакозана (Рис. 4) также включает восемь серий ионов, но по сравнению со спектром 1-бром
нонаном (Рис. 3) при увеличении массы алкильной цепи на 224 а.e.м., в нем происходит трехкратное
снижение интенсивности пика +C4H8Br с m/z 135 и смена максимального
пика алкильного иона +C3H7 (72%) на базовый пик +C4H9 (100%). Рисунок 4. Восемь серий ионов масс-спектра 1-бром пентакозана C25H51Br MW: 430 Зависимости интенсивностей (I отн.%) четырех алкильных и двух бромалкильных пиков спектров гомологов
С1-С34 алкилбромидов от числа углеродных атомов алкильной цепи (массы алкильной
цепи) представлены на (Рис. 5). Рисунок 5. Зависимости интенсивностей (I отн.%) пиков в спектрах алкилбромидов В спектрах гомологов C3-C8 происходит смена базовых алкильных ионов. В C3 и C4 (43- в C3, 57- в C4) она результат отрыва атома .Br.
В спектрах C5 и C8, после отрыва .Br, смена базовых алкильных ионов
результат последующей фрагментации возникающих алкильных ионов +C5H11-+C8H17,
фрагментирующих с отрывами C2H4 или C3H6. В спектре C5, при отрыве метильного радикала, образуется слабый пик +C4H8Br
m/z 135 (0.2%). В спектрах C6-C8 интенсивность его увеличивается до 86%, а
интенсивность пиков M-Br снижается с 51 до 2.3%. Тем ни менее в спектрах C7-C8 пик алкильного иона с m/z 57 остается базовым. Главными фрагментационными процессами, происходящими
в спектрах C3-C8 являются: +C3H7Br - .Br → +C3H7 m/z
43 (100%) +C4H9Br. - .Br → +C4H9 m/z 57 (100%) +C5H11Br - .Br → +C5H11 m/z 71 (84%) - C2H4 → 43 (100%) +C5H11Br - .CH3 → +C4H8Br
m/z 135 (0.2%) +C6H13Br - .Br → +C6H13 m/z 85 (51%) - (C3H6) → +C3H7 m/z 43 (100%) +C6H13Br - .C2H5 → +C4H8Br
m/z 135 (42%) +C7H15Br - .Br → +C7H15 m/z 99 (0.2%) - (C3H6) → +C4H9 m/z 57 (100%) +C7H15Br - .CH3 + C2H4 →
+C4H8Br m/z 135 (54%) +C7H15Br - .C2H5 → +C5H10Br
m/z 149 (3%) +C8H17Br - .Br → +C8H17 m/z 113 (2.3%) - (C3H6) → +C5H11 m/z 71 (78%)
+C8H17 m/z 113 (2.3%) - (C2H4) → +C6H13 m/z 85 (2.3%) +C6H13 m/z 85 (2.3%) - (C2H4) → +C4H9 m/z 57 (100%) +C8H17Br - .C2H5 + C2H4 → +C4H8Br m/z 135 (86%) +C8H17Br - .CH3 + C2H4 →
+C5H10Br m/z 149 (10%) В спектрах гомологов C8-C12 (Рис. 5) базовым пиком становится пик +C4H8Br
m/z 135. Интенсивность пика M-Br снижается до 2.3% в C8 и 0.7% в C12. Почти
полное прекращение отрывов брома становится причиной снижения интенсивностей пиков базовых алкильных
ионов +C3H7, +C4H9 и +C5H11,
поскольку для их возникновения необходим отрыв .Br. Начиная с гомолога C13,
происходит достаточно резкий спад интенсивности пика +C4H8Br, обратно
пропорциональный росту соотношения массы бромалкильной цепи (M- 135 100%) к массе ее наиболее интенсивного
иона с m/z135 (график фиолетового цвета). Менее резко происходит спад интенсивности пика +C5H10Br,
имеющего большую массу. В спектрах гомологов C14‑C25 начинается рост интенсивности
пика M-Br, базовым пиком спектра снова становится +C4H9. Когда
масса алкильной цепи (M- 135) становится больше массы максимального бромалкильного иона+C4H8Br
m/z 135, происходит снижение интенсивности его пика, поскольку стабилизация атома брома распространяется
на всю алкильную цепь от M+. до иона с m/z 135. Рисунок 6. Восемь серий ионов масс-спектра 1,20-дибром эйкозана C20H40Br2 MW:438 Спектр 1,20-дибром эйкозана (Рис. 6) включает восемь серий ионов, каждая из которых завершается
пиком, имеющим в данной серии максимальную интенсивность (m/z 57, 43, 56, 42, 55, 69 и 135, 149).
В обеих алкильных сериях спектра 1,20-дибром эйкозана, после отрыва двух атомов брома, также как и при
фрагментации циклоалканов [4], происходит выброс винильного радикала с образованием терминальной
метильной группы. В трех сериях ионов 1,20-дибром эйкозана (Рис. 6.): в одной из алкильных серий
(с максимальным пиком m/z 43), в одной из олефиновых серий (с максимальным пиком m/z 42), а также
в одной из бромалкильных серий (с максимальным пиком m/z 149), содержащих нечетное число метиленовых
групп, происходят выбросы пропилена. По сравнению с масс-спектром 1-бром эйкозана (Рис. 2) в спектре
1,20-дибром эйкозана (Рис. 6) интенсивность пика +C4H8Br снижается
более чем в два раза с 53% до 22%. Причиной такого понижения интенсивности пика с m/z 135 по‑видимому,
является двухкратное увеличение вероятности отрыва атомов брома. Влияние массы отрываемого галогенида на интенсивность пика [М+.- .Hal]+ в масс-спектрах 1,4-дигалогенбутанов Современные работы по изучению влияния молекулярной массы гомологов на их фрагментацию и интенсивность
образующихся характерных и базовых ионов практически отсутствуют. Исключением является МС/МС исследование
фрагментации пептидов, в котором авторами [5] обнаружено влияние массы пептида на рост и снижение
количеств ионов, а также интенсивностей их пиков в сериях двух разных типов: -y и –b, образующихся
в результате разрывов пептидной цепи. Очередность отрыва алкильных заместителей в N‑(трет-алкил)-аминах
и -ацетамидах в соответствии с возрастанием их масс, а также рост интенсивности пиков ионов, образующихся
при увеличении массы отрываемых алкильных радикалов описаны как «эффект ионной массы» и количественно
рассчитаны в работе Загорского [6]. В отечественных обзорах по масс-спектрометрии этот эффект называют
правилом выброса максимального алкильного радикала [7]. Примеры применения правила для случаев, когда
масса суммарного отрываемого радикала больше массы образующегося иона, по-видимому, отсутствуют. Влияние молекулярной массы отрываемого атома галогенида на интенсивность образующегося пика M+. -
.Hal = +C4H8Hal подтверждается спектрами
α,ω-дигалогенбутанов: 1,4-дииод-, 1,4-дибром- и 1,4-дихлор- и 1,4-дифтор бутанов (Табл. 1). Таблица 1. Интенсивности пиков +C4H8Hal в спектрах α,ω-дигалогенбутанов I % и их расчетные значения % Hal, соответствующие отрываемым массам галогенидов. Масс-спектр C4H8Hal2 Library Formula: MW и - Hal % I % пика +C4H8Hal в спектре % Hal / m/z I Бутан, 1,4-дииод- ID#:259815 DB:wiley nist98 C4H8I2 MW 310 - I 41% m/z 183 100% m/z I 127 100% Бутан,1,4-дибром- ID#:134901 DB:wiley nist98 C4H8Br2 MW 214 - Br 37% m/z 135 63% Br 79 - 62,2% Бутан, 1,4-дихлор- ID#:20972 DB#: mainlib C4H8Cl 2 MW 126 -Cl 28% m/z 90 30% Cl 35 - 27,6% Бутан,1,4-дифтор- Нет спектра C4H8F2 MW 96 - F 20% m/z 75 ? % F 19 - 15% В спектре C4H8I2 (Табл. 1), при отрыве радикала I. образуется
базовый пик с m/z 183 (M-127). При отрывах атомов брома и хлора интенсивности пиков M+.-.Hal
(Табл. 1) снижаются до 63% и 30% соответственно. Снижение интенсивностей происходит пропорционально молекулярным массам отрываемых .Hal,
относительно массы атома иода принятой за 100%. Интенсивности пиков образующихся ионов +C4H8Hal
(Табл. 1) соответствуют значениям масс отрываемых атомов .Hal. Поскольку
отрыв атома галогена от α,ω-дигалогеналкана является первичным процессом, энергия M+. достаточна для разрыва любой связи C4H8Hal2. По сравнению с эффектом
отрыва массы галогенида, приводящим к снижению колебательного возбуждения и росту интенсивности пика
образующегося иона, различие в энергиях связей отрываемых атомов галогенидов, за исключением фтора,
в спектрах α,ω-дигалогенидов, не оказывает существенного влияния на интенсивность образующегося пика.
При разрывах наиболее слабых связей СН2-I и CH2-Br избыточная колебательная
энергия вероятно должна приводить не к росту, а к снижению интенсивности пиков +C4H8I
и +C4H8Br. Однако этого не происходит. Выбор именно спектров C4 (таблица
1) сделан не случайно. Если в масс-спектре BrC4H8Br отрыв любого
из двух терминальных атомов брома приводит к возникновению стабильного иона +C4H8Br
(42%), то в спектрах дибромалканов С5-С6 возникает некий конфликт интересов
терминальных атомов Br за обладание большим числом метиленовых групп, обусловленный встречными фрагментациями.
Он приводит к образованию в спектрах С5-С6 новой серии ионов M-HBr и резкому
понижению интенсивности пика иона +C4H8Br (0,4% - 1,8%). Данный
конфликт несколько ослабевает в спектре C7, в котором интенсивность пика +C4H8Br
всего 16%. Полностью конфликт прекращается только в C8, когда пик иона +C4H8Br
может образоваться при распаде M+./2, в результате отрыва
радикала Br(CH2)3CH2+.CH2(CH2)3Br
→ +C4H8Br + .C4H8Br.
Однако, при этом интенсивность пика +C4H8Br в спектре C8,
по сравнению с C4, снижается почти в два раза – до 29%. Вероятной причиной снижения интенсивности
пика +C4H8Br является двухкратное увеличение вероятности отрыва
атома .Br. Влияние массы отрываемого галогенида на интенсивность пика [М+.- .Hal]+ в масс-спектрах 1,4-дигалогенперфторбутанов Сходный эффект влияния массы отрываемого радикала .Hal на интенсивность образующегося
фрагментного иона M+. - .Hal наблюдается
и в спектрах α,ω-дигалогенперфторбутанов (Табл. 2). Таблица 2. Интенсивности пиков +C4F8Hal в спектрах дигалогенперфторбутанов I % и их расчетные значения % Hal, соответствующие отрываемым массам галогенидов. Масс-спектр C4F8Hal2 Library Formula: MW и M Hal % I % пика +C4F8Hal В спектре % Hal / m/z I 1,4-дииод-октафторбутан ID#:230290 DB: mainlib C4F8I2 454 -I (28 %) m/z 327 100% m/z I 127 100% 1,4-дибром- октафторбутан Polaris Q C4F8Br2 358 -Br (22%) m/z 279 62% Br 79 62,2% 1,4-дихлор- октафторбутан Polaris Q C4F8Cl 2 270 -Cl (13%) m/z 235 8,3% Cl 35 27,6% Перфтор н-бутан- ID#:36162 DB#: mainlib C4F10 238 -F (9%) m/z 219 2,6% F 19 15% В масс-спектре C4F8I2 (Табл. 2), при отрыве радикала I. образуется
базовый пик с m/z 327 (M-127). При отрывах атомов брома и хлора интенсивность пика M+.-.Hal
(Табл. 2) снижается до 62% и 8% соответственно. Если снижение интенсивностей пиков, образующихся
при отрывах атомов I и Br происходит пропорционально их молекулярным массам, то при отрывах атомов
Cl и F снижение интенсивностей пиков происходит в три и, соответственно, в пять раз больше ожидаемых
значений интенсивностей, пропорциональных отрываемым массам атомов Cl и F. Следует отметить, что эффект отрыва массы галогенида зависит также от массы цепи (алкильной или перфторалкильной).
Чем больше масса цепи и масса образующегося иона тем меньше эффект отрыва атома галогенида. В Таблицах
1 и 2, в графе MW представлены значения масс отрываемых атомов галогенов в % от молекулярного веса
соединений. Процентные значения масс атомов Cl и F в соединениях с перфторалкильной цепью C4 в 2,2 раза меньше процентных значений их масс в соединения с алкильной цепью (Табл. 1 и 2). Тогда
как отрыв масс I и Br от перфторалкильной цепи C4 по сравнению с отрывом от алкильной
цепи меньше только в 1,5 и 1,7 раза соответственно. Эффект отрыва от перфторалкильной цепи галогенидов
с минимальными массами (Cl и F) по сравнению с отрывом галогенидов с максимальными массами (Br и
I) соответственно должен быть меньше. Представленные примеры отрыва атомов .Hal
от перфторалкильной цепи подтверждают влияние массы отрываемого радикала и массы цепи на интенсивность
образующегося иона. Эффекты отрыва атома брома в масс-спектрах н-алкилбромидов и α,ω-дибромалканов
Эффекты отрыва массы атома брома на интенсивности алкильных и бромалкильных пиков можно оценить, сравнив
спектры н-алкилбромида и α,ω-дибромалкана, содержащих одинаковое число углеродных атомов. Рисунок 7. Масс-спектры 1-бром додекана C12H25Br MW:248 ID#: 183675 DB#: wiley_nist 98 По сравнению с масс-спектром 1-бром додекана в спектре 1,12-дибром додекана (Рис. 7) интенсивность пика
+C4H8Br с m/z 135 снижается более чем в два раза до (42,5%), а интенсивность
пика +C5H10Br с m/z 149 почти не меняется. Усиливается слабый пик
+C6H12Br с m/z 163 (11,3%), который в спектре C12H24Br2 может возникать при распаде M/2 и появляются бромсодержащие пики, не проявлявшиеся в спектре 1-бром
додекана. Наибольшую интенсивность приобретает пик+.M-.Br
(26,1%) с m/z 247. Ионы с m/z 135 и m/z 149 образуются в двух разных ионных сериях, по этой причине
изменение интенсивности одного из пиков может и не приводить к изменению интенсивности пика другой
серии. В отличие от несимметричной молекулы 1-бром додекана, снижение в два раза интенсивности пика
с m/z 135 в спектре 1,12-дибром додекана результат двухкратного увеличения вероятности отрывов атома
брома. Отрывы двух атомов брома, происходящие в четырех сериях спектра (Рис. 6) снижают вероятность
образования пика +C4H8Br и повышают интенсивности серий алкильных
и алкенильных ионов (Рис. 7). Усиление интенсивности бромсодержащих фрагментных пиков с m/z 247,
205, 191, 177 - результат стабилизирующего влияния масс двух терминальных атомов, снижающих колебательное
возбуждения +.M в два раза сильнее, чем один терминальный
атом Br. Рисунок 8. Масс-спектры 1-бром гексадекана C16H33Br MW:304 NIST#: 228693 ID#: 24350 В отличие от спектра 1,12-дибром додекана (Рис. 7) содержащего семь бромалкильных иона, в спектре 1,16-дибром
гексадекана (Рис. 8) серия состоит из одиннадцати бромалкильных ионов, однако интенсивности их в
два раза ниже. Снижение интенсивностей галогенсодержащих пиков при увеличении массы цепи происходит
в результате снижения стабилизирующего влияния фиксированной массы атома галогенида, распределяющегося
на всю цепь от +.M до +C4H8Hal. При увеличении
алкильной цепи на четыре метиленовых группы с С12 до С16 снижение интенсивности
пика с m/z 135 (24,7%) в спектре 1,16- дибром гексадекана по сравнению со спектром 1-бром гексадекана
(41,6%) (Рис. 8) происходит почти также, как в спектре 1,12-дибром додекана (Риc. 7). Ионные серии масс-спектров α,ω-дигалогенперфторалканов Три серии ионов: перфторалкильная, перфторалкенильная и перфторолефиновая масс-спектра
перфторэйкозана NIST#:239239 ID#:36518 DB:mainlib рассмотрены ранее [2,4]. Масс-спектры α,ω-дигалогенперфторалканов
состоят из четырех серии ионов (Рис. 9-12) перфторалкильной (+CF3 m/z 69),
перфторалкенильной (+C3F5 m/z 131), галогенперфторалкильной (+CF2Hal)
и галогенперфторалкенильной серии (+C3F4Hal). Ионы галогенперфторалкенильной
серии, возникающие в результате отрыва атома галогенида (Cl или Br) и выбросов двух атомов фтора
могут иметь как линейное, так и циклическое строение. Рисунок 9. Четыре серии ионов масс-спектра 1,6-дихлор перфторгексана C6 Cl2F12 MW:370 NIST#: 394371 ID#: 55090 DB: mainlib. Алкенильная серия (M- 2.Cl - .F- (CF2)n m/z 131, на данном рисунке не представлена. Однако последовательные отрывы CF2, происходящие в галогеналкенильной серии несовместимы с
ее линейной структурой и концевой группой -CF=+CF. Последовательный рост интенсивностей
пиков этой серии, с максимумом при m/z 147 +C3F4Cl 10% (в спектре
C16Cl2F32 MW:870 Polaris Q интенсивность пика с m/z 147 39%), позволяют
предполагать, что все ионы кроме завершающего линейного иона CF2=+CCl m/z 97
имеют циклическое строение (Рис. 9). Аналогичные фрагментационные процессы происходят в спектре 1,7‑дибром
перфторгептана (Рис. 10.), в котором интенсивность пика +C3F4Br,
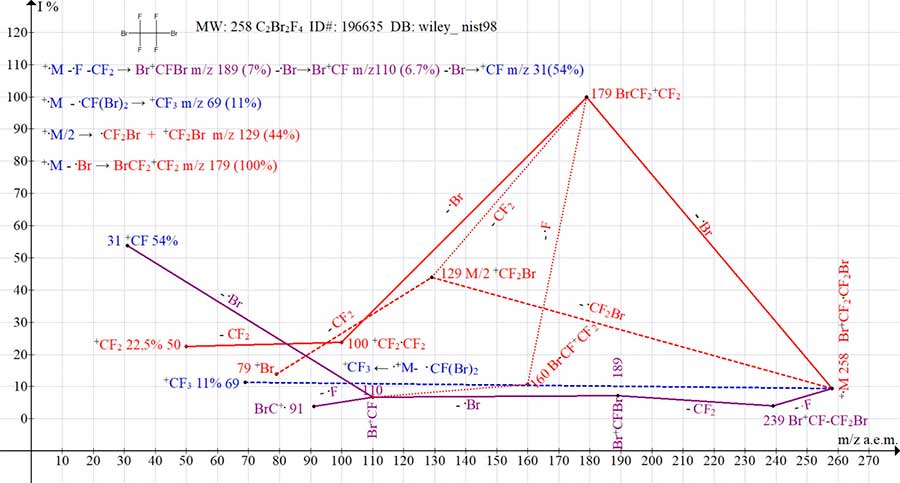
с m/z 191 (11%). Однако, в масс-спектре 1,2-дибром тетрафторэтана (Рис. 11), из-за слишком близкого
расположения терминальных атомов брома и взаимной стабилизации их масс, отрывов атома брома и 2-х
атомов фтора не происходит и ион Br+C=CF2 галогеналкенильной серии с m/z 141
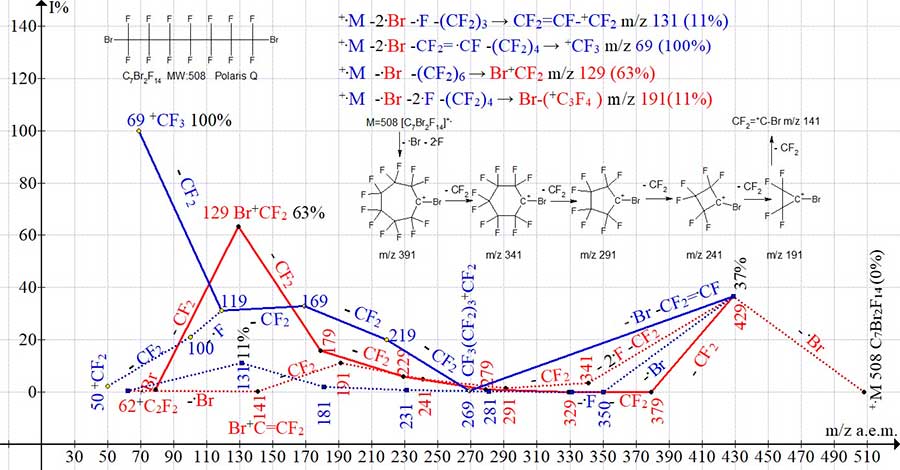
не образуется. Рисунок 10. Четыре серии ионов масс-спектра 1,7-дибром перфторгептана C7Br2F14 MW:508 Polaris Q. Рисунок 11. Четыре серии масс-спектра 1,2-дибром -1,1,2,2- тетрафторэтана C2Br2F4 MW:258 ID#: 196635 DB: wiley_nist98. Вместо этого, в результате выброса атома фтора и отрыва CF2 возникает ион Br-+CF-Br
m/z189 (7%), а при отрыве радикала Br-.CF-Br перегруппировочный ион +CF3 (11%). Отрыв атома брома от иона Br-+CF-Br (Рис. 11) не приводит к росту интенсивности
образующегося иона Br-+CF, поскольку это не первичный отрыв, а затратный процесс, разрушающий
взаимную стабилизацию масс двух атомов брома. Однако, заключительный отрыв атома брома с образованием
иона +CF приводит к резкому росту интенсивности его пика (54%). В спектре гомолога C4F8Br2 (Рис. 13), из-за отдаленности масс терминальных атомов брома, пик иона Br-CF2+CFCF2-Br
с m/z 289 не образуется. В спектре дихлортетрафторэтана MW: 170 C2Cl2F4 ID #: 72335 (wiley_nist98) образуется ион Cl+CFCl m/z 101 (13%). Но в спектре 1,2-дийодтетрафторэтана
MW: 354 C2F4I2 ID #: 301040 DB: wiley_nist98 ион I+CFI не образуется. Вместо этого появляется
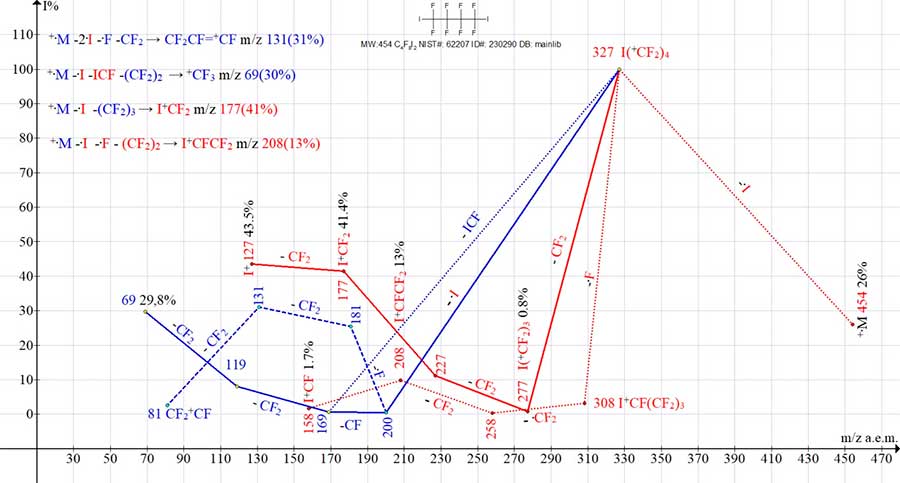
интенсивный пик I2 m/z 254 (48%) +.M-C2F4. Рис.12. Четыре серии ионов масс-спектра перфтор 1,4-дииодперфторбутана C4F8I2 MW:454
NIST#: 62207 ID#: 230290 DB: mainlib. В масс-спектрах α,ω-дигалогенперфторалканов (Рис. 9-12) при отрыве терминального атома галогена образуется
первичный галогеналкильный ион, интенсивность которого зависит от массы галогенида и массы цепи.
Максимальную интенсивность приобретает пик иодсодержащего иона +.M-.I
(Рис.12), а минимальную хлор-содержащий ион +.M-.Cl
(Рис. 9), что соответствует массам отрываемых галогенидов. При фрагментации первичного галогенсодержащего
иона происходит резкое снижение интенсивности его пика, однако последующие отрывы CF2 приводят к серии возрастающих пиков ионов, завершающейся наиболее интенсивным пиком Hal+CF2.
Стабилизируемые атомами галогенидов минимальные массы алкильной и перфторалкильной цепи, близки по их
величине: m/z 56 а.e.м. в алкильной цепи и m/z 50 а.e.м. в перфторалкильной цепи, что соответствуют
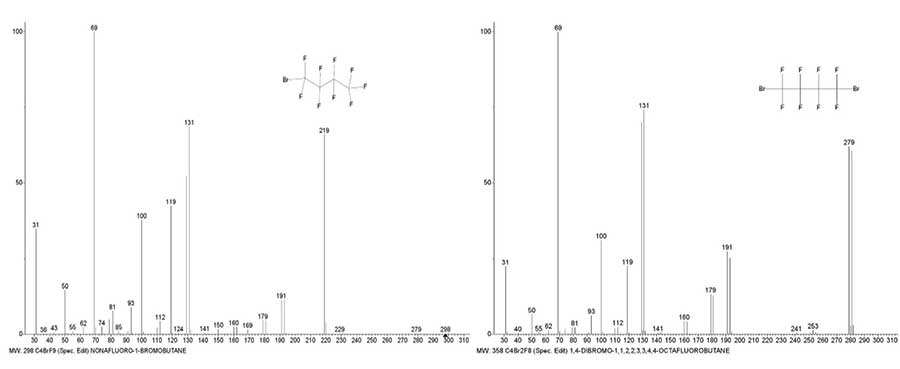
массами двух этиленовых (C2H4)2 групп или одной CF2. Рисунок 13. Масс-спектры 1-бром нонафторбутана C4BrF9 MW:298 NIST#: 222723 В масс-спектрах 1-бром нонафтор и 1,4-дибром октафтор бутанов (Рис. 13) при первичнных отрывах атома
фтора и соответственно атома брома образуется один и тот же ион Br(+CF2)4 с m/z 279. Интенсивность пика Br(+CF2)4, возникающего при отрыве
.F (0.2%), что в 310 раз меньше интенсивности пика, при отрыве атома
.Br (62%). Отрыв атома брома в спектре 1-бром нонафтор бутана приводит
к образованию и стабилизации интенсивного пика иона +C4F8 с m/z
219 (66%). В спектре C4BrF9 атом брома стабилизирует ионы Br+C2F4 (5%) и Br+CF2 (52%). В отличие от этого, отрыв атома брома от C4Br2F8 позволяет стабилизировать всю бромперфторалкильную цепь. Чем больше масса первичного отрываемого
радикала, тем меньшую долю избыточной энергии M.+ получает возникающий
ион, что способствует росту интенсивности его пика. В отличие от масс-спектров α,ω-дибромалканов (Рис.
7-8) в которых, по сравнению со спектрами α-бромалканов, из-за встречной фрагментации происходит
двухкратное снижение интенсивности пика Br+C4H8 m/z 135, в спектрах
α,ω-дибромперфторалканов, по сравнению со спектрами соответствующих монобромперфторалканов, происходит
рост пиков Br(+CF2)2 (13%) и Br+CF2 (70%).
Этот факт позволяет заключить, что, в отличие от алкильных цепей, в перфторалкильных цепях (Рис. 7‑8)
встречная фрагментация, по-видимому, не происходит. Обратно пропорциональное влияние массы перфторалкильной цепи на интенсивность пика отрываемого галогенида
иллюстрируют зависимости интенсивностей пиков +.M и +.M-.I
спектров гомологов иодперфторалканов от их молекулярной массы (Рис. 14). С ростом молекулярной массы
гомологов н-пефториодидов интенсивность пика M-I снижается пропорционально уменьшению относительной
доли массы атома иода в молекуле н‑перфториодида. Чем больше молекулярная масса гомолога, тем меньшее
влияние на фрагментацию оказывает отрыв атома иода. Рисунок 14. Зависимости интенсивностей (I отн.%) пиков в спектрах перфторалкилиодидов от молекулярной массы гомологов (C3-C10 296-646). (C3F7I MW:296 NIST#: 235506 ID#: 157700 ; C4F9I MW:346 NIST#: 376328 ID#: 195259; C6F13I MW:446 NIST#: 239055 ID#: 36897; C7F15I MW:496 NIST#: 118317 ID#: 36933; C8F17I MW:546 NIST#: 238726 ID#: 36511; C10F21I MW:646 NIST#: 239284 ID#: 36183; DB: mainlib О постепенном росте пиков последовательно фрагментирующих ионов. Касаясь проблемы постепенного роста интенсивности всех пиков последовательно фрагментирующих ионов, в
спектрах эйкозана C20H42, гексаконтана н-C60H122, циклотриаконтана
C30H60, перфторэйкозана C20F42 следует отметить, что
незначительный, постепенный и последовательный рост пиков обычно мы не замечаем. Внимание исследователей,
как правило, обращено на пики c максимальной интенсивностью, а также перегруппировочные пики ионов.
Высокую интенсивность пиков объясняют только энергетической выгодностью, структурной изомеризации
или циклизации [7]. Действительно, расчетные значения энтальпий образования алкильных ионов, содержащих третичный атом углерода
на 18-30ккал/моль меньше чем энтальпии соответствующих линейных ионов [8]. Энтальпии образования ΔHf (г) 298K углеводородных ионов (ккал/моль), [8, стр.199]. Алкильные ионы M/Z ∆Hf 0 (ккал/моль) CH3CH2+CH2 +CH(CH3)2 43 207 189 207-189=18 CH3CH2CH2+CH2 +C(CH3)3 57 201 168,5 201- 168,5=32,5 CH3CH2CH2CH2+CH2 +CH(CH2CH3)2 71 данные отсутствуют 172,6 Тем не менее, все наиболее интенсивные алкильные пики c m/z 99, 85, 71, 57 н‑алканов фрагментируют только
последовательными отрывами C2H4, что не вполне согласуется с предположением
о их перегруппировках и отличается от высокой устойчивости +C(CH3)3 в масс-спектрах с заведомыми третичными группами. В отличие от спектров н-алканов, состоящих из шести
серий пиков (Рис. 1), в масс-спектрах линейных алканов, с терминальной группой C(CH3)3,
число основных серий уменьшается до трех. Главными путями их фрагментации являются: выброс линейного
радикала с образованием пика базового иона +C(CH3)3, выброс радикала
.C(CH3)3 с образование алкильного иона, включающего
всю алкильную цепь, а также отрывы .C(CH3)3 и .H
с образованием алкильного иона с терминальной винильной группой. Постепенный рост интенсивностей
пиков всех фрагментных ионов, сложно объяснить их синхронно возрастающей структурной стабилизацией,
однако с уменьшением длины цепи линейного иона вероятность циклизаций или перегруппировок, безусловно,
увеличивается. В двух разных сериях галогенсодержащих ионов масс-спектров н-алкилгалогенидов только
два иона +C4H8Hal и +C5H10Hal,
завершающих фрагментацию, интенсивности пиков которых максимальны, по сравнению с интенсивностями
остальных пиков линейных Hal-содержащих ионов - являются перегруппировочными ониевыми ионами, циклическое
строение которых подтверждено экспериментально [9]. Постепенный рост интенсивностей всех последовательно
фрагментирующих пиков ионов н-алканов и циклоалканах происходит синхронно с выбросами этилена и перераспределением
(передачей) части его кинетической энергии (по принципу пушка-снаряд) новому алкильному иону с меньшей
массой. То есть в общем случае, если не рассматривать случаи перегруппировки или циклизации, интенсивность
пика зависит от соотношения массы и энергии образующегося иона к массе и энергии постоянной отрываемой
группы этилена. Для описания такой системы, которой является молекулярный катион-радикал, выстреливающий
молекулами этилена, следует учитывать две его составляющих [10]. Во-первых, скорость движения M+.,
как скорость движения центра инерции всей системы, а также скорость внутреннего движения - отрываемого
первичного радикала (или выбрасываемого этилена), и скорость нового возникающего иона. В соответствии
с этим энергию системы можно представить в виде суммы кинетической энергии M+. (или
энергии любого фрагментного иона как целого) и кинетических энергий движения новых частиц: иона и
этилена, образующихся в результате единичного акта распада. При отрывах первичных радикалов, имеющих различные массы, избыточная энергия молекулярного катион-радикала
н-алкана, составляющая около 20эВ = 460 ккал/моль, делится шестью способами между первичными ионами
и радикалами шести соответствующих серий фрагментаций. Сложность расчета перераспределения кинетической энергии между фрагментными ионами и этиленом состоит
в том, что нам известны массы ионов и интенсивности их пиков, но неизвестны их скорости. По этой
причине выполнить подобный расчет не представляется возможным. Чтобы оценить, как в ходе фрагментации
происходит перераспределение энергии между фрагментными ионами и этиленом, расчет можно сделать в
упрощенном виде, воспользовавшись значениями интенсивностей. Интенсивности пиков масс-спектра зависят
от энергии ионизирующего напряжения и при различных значениях ионизирующего напряжения отражают различные
варианты перераспределений энергии. Стандартные условия съемки масс-спектров (70эВ) минимизируют
эту зависимость, но существующая связь между энергиями ионов и интенсивностями их пиков сохраняется.
Поскольку интенсивность пика определяется ионным током, (количеством ионов, имеющих одинаковую структуру
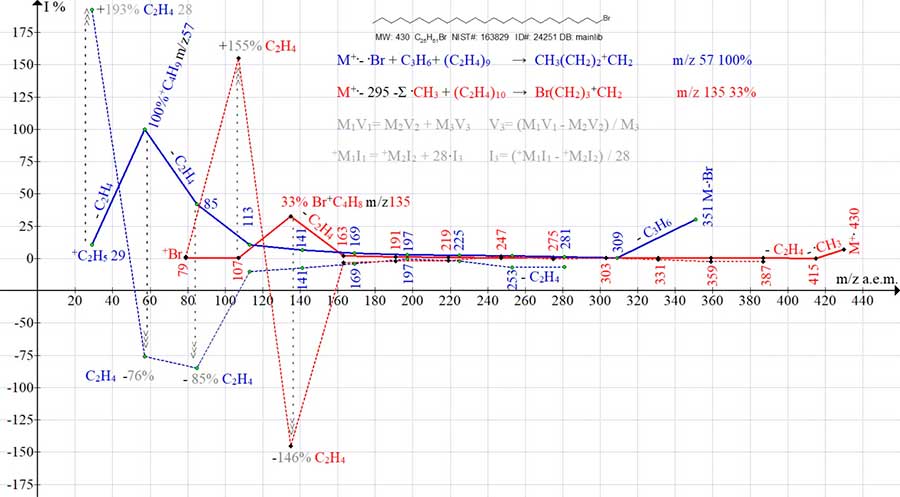
и кинетическую энергию), она пропорциональна энергии. По формуле закона сохранения импульса [11],
в которой вместо скоростей брались интенсивности пиков двух главных алкильных серий ионов масс-спектра
эйкозана C20H42, были рассчитаны значения фиктивных интенсивностей выбрасываемых
нейтральных молекул этилена (2). +M1I1= +m2 i2 + 28 Iфикт.этилена (2) В отличие от изменяющихся масс фрагментных ионов, масса этилена постоянна, 28 а.e.м.. По этой причине
любое изменение фиктивной интенсивности этилена, не соответствующее интенсивности пика данного алкильного
иона указывает на возможность его перегруппировки, циклизации или распада. Найденные значения фиктивных
интенсивностей этилена, пропорциональные интенсивностям и массам последовательно образующихся ионов
масс-спектра эйкозана представлены на (Рис. 15). Для упрощения задачи, шесть первичных вариантов
фрагментации M+. (Рис. 1), деления интенсивности (энергии)
M+. шестью способами между шестью отрываемыми радикалами и
шестью первичными ионами на (Рис. 15) не представлены. Два верхних положительных графика (+ линии
красного и синего цвета) (Рис. 15) - графики масс - интенсивностей двух главных алкильных серий ионов
после отрыва .CH3 и .C2H5 и
выбросов этилена. Они завершаются интенсивным пиком иона с m/z 71 и базовым пиком с m/z 57. Нижние
графики- графики фиктивных интенсивностей этилена (пунктирные линии), в интервале масс от 230 до
113 и 99 а.e.м. зеркально повторяют симметричный и последовательный рост, противоположно направленный
росту верхних графиков интенсивностей алкильных ионов. Что дает основание заключить, что в этом интервале
масс перегруппировок нет, а только идет последовательный рост энергии ионов и фиктивных интенсивностей.
Рисунок 15. Две серии интенсивностей последовательно фрагментирующих алкильных ионов масс-спектра эйкозана C20H42 MW: 282 (+ графики красного и синего цвета) и две серии их фиктивных интенсивностей этилена (- пунктирные графики красного и синего цвета). При соотношении масс (пушка-снаряд 85:28 = 3:1) интенсивному пику иона с m/z 85 (60,5%) соответствует
в два раза превышающая его фиктивная интенсивность этилена (‑128%), подтверждающая энергетическую
выгодность процесса. Однако, при следующем отрыве этилена и соотношении масс 57:28 = 2:1 возникает
базовый пик с m/z 57, а фиктивная интенсивность этилена резко снижается до -20 %. Причиной такого
снижения, отличающегося от всех предшествующих отрывов этилена, может являться экзотермический эффект
перегруппировки линейного иона в третичный. Завершающий выброс этилена при соотношении масс 1:1 приводит
к образованию иона +C2H5 с низкой интенсивностью (9%), смене полярности
и росту значения фиктивной интенсивности этилена (+194%). Причиной смены полярности, вероятно, является обратная перегруппировка третичного иона +C(CH3)3 m/z 57 в линейный и его распад с отрывом этилена. При соотношении масс 71:28 = 2.5:1 максимуму интенсивности
иона +C5H11 m/z 71 (+77%) соответствует максимум фиктивной интенсивности
этилена +C2H4 (-124%). Следующий отрыв этилена понижает интенсивность
пика иона +C3H7 до 64%. При соотношении масс 43:28 = 1.5:1 происходит
резкая смена полярности фиктивной интенсивности этилена +98%, что, по-видимому, результат обратной
перегруппировки симметричного иона CH3CH2+CHCH2CH3 в несимметричный линейный. Соотношение положительных значений фиктивных интенсивностей этилена для
ионов с m/z 29 и m/z 43 равно 194: 98. Действительно, для перегруппировки иона CH3CH2+CHCH2CH3 в ион CH3 (CH2)3+CH2, с миграцией одного протона,
вероятно требуется меньше энергии, чем для перегруппировки в линейный ион третичного иона +C(CH3)3. Еще один пример постепенного роста и смены полярности фиктивных интенсивностей этилена в двух параллельных
сериях ионов масс-спектра 1-бром пентакозана иллюстрируют графики интенсивностей его главной алкильной
серии с базовым алкильным ионом +C4H9 m/z 57 и главной бромалкильной
серии с ионом +C4H8Br m/z 135 (Рис. 16). Следует отметить, что ион
+C4H8Br – перегруппировочный ион, циклическое строение которого
подтверждено экспериментально [9]. Рисунок 16. Две серии последовательно фрагментирующих ионов масс-спектра При соотношении масс m/z 135:28 = 4.8:1 максимуму интенсивности иона +C4H8Br m/z
135 (+33%) соответствует максимум фиктивной интенсивности этилена +C2H4 (-146%).
В отличие от всех предшествующих линейных бромалкильных ионов, только при образовании иона +C4H8Br
происходит выигрыш энергии, обусловленный циклизацией иона. Однако, при следующем отрыве этилена
интенсивность пика иона +C2H4Br m/z 107 снижается до
0.5%, а фиктивная интенсивность выбрасываемого этилена резко меняет полярность (+155%). Такое изменение
полярности соответствует затратам энергии на разрыв циклического иона и отрыв от него этилена. Несмотря
на то, что по сравнению с ионами алкильной серии ион с m/z 107 имеет достаточно большую массу, при
следующем отрыве от него этилена с образованием иона брома возникает дефицит энергии (+1.3%). Значения
фиктивных интенсивностей этилена (+155 и +193, Рис. 16) при отрывах от циклического галониевого иона
+C4H8Br [9] и иона +C(CH3)3 подтверждают,
что для отрыва этилена от +C4H8Br необходима меньшая затрата энергии,
чем для обратной перегруппировки +C4H9 в линейный ион и отрыва от
него этилена. Очевидно, что энергия раскрытия ониевого цикла, безусловно, меньше энергии, необходимой
для обратной перегруппировки третичного иона +C(CH3)3 в линейный
с миграцией двух протонов. Анализом масс-спектров эйкозана C20H42, 1-бром эйкозана и 1,20-дибром эйкозана
установлены последовательности их распада - шесть и соответственно восемь ионных серий. В масс-спектрах
α,ω-дигалоген перфторалканов установлены четыре ионных серии. Предложен графический метод фиктивных
интенсивностей этилена, позволяющий различать зоны масс-спектра, где происходит последовательный
рост интенсивностей, в связи с увеличением энергии ионов, и зоны где происходят перегруппировки ионов
и их распад. Графики фиктивных интенсивностей этилена позволяют заключить, что базовый ион +C4H9 -
третичный ион +C(CH3)3, который при завершающем отрыве этилена снова
превращается в линейный. Ион +C4H8Br - базовый ион гомологов С9-С12,
отличается от базового иона +C4H9 тем, что содержит массивный атом
брома, стабилизирующий всю серию бромалкильных ионов от M+. до +C4H8Br, а также и его слабые фрагментные ионы. По этой причине
при увеличении массы стабилизируемой алкильной цепи интенсивность пика +C4H8Br
снижается и увеличивается вероятность отрыва атома брома. На примерах масс-спектров α,ω-дигалогенбутанов и α,ω-дигалоген перфторбутанов подтверждено, что интенсивность
пика иона, образующегося при отрыве терминального галогенида прямо пропорциональна массе отрываемого
галогенида и обратно пропорциональна массе алкильной или перфторалкильной цепи. Независимо от структурной стабилизации рост интенсивностей всех пиков ионов н-алканов, циклоалканов,
перфторалканов и перфторциклоалканов происходит при уменьшении их масс, синхронно с перераспределением
энергии возбуждения, в результате последовательных выбросов [C2H4]n или [CF2]n. В общем случае, интенсивность пика зависит от соотношения массы
иона к массе постоянной отрываемой группы. Максимальные интенсивности предпоследних пиков алкильных
ионов завершающих фрагментацию обусловлены как оптимальными соотношениями их масс и энергий, так
и возрастающей возможностью их циклизации или перегруппировки. Представленные зависимости фиктивных
интенсивностей этилена, позволяют заключить, что +C4H9 также как
и +C4H8 Hal является перегруппировочным ионом. Работа выполнена при поддержке Министерства науки и высшего образования Российской Федерации с использованием
научного оборудования Центра исследования строений молекул ИНЭОС РАН. Статья рекомендована к публикации к.х.н. О.В. БрызгаловойЭкспериментальная часть
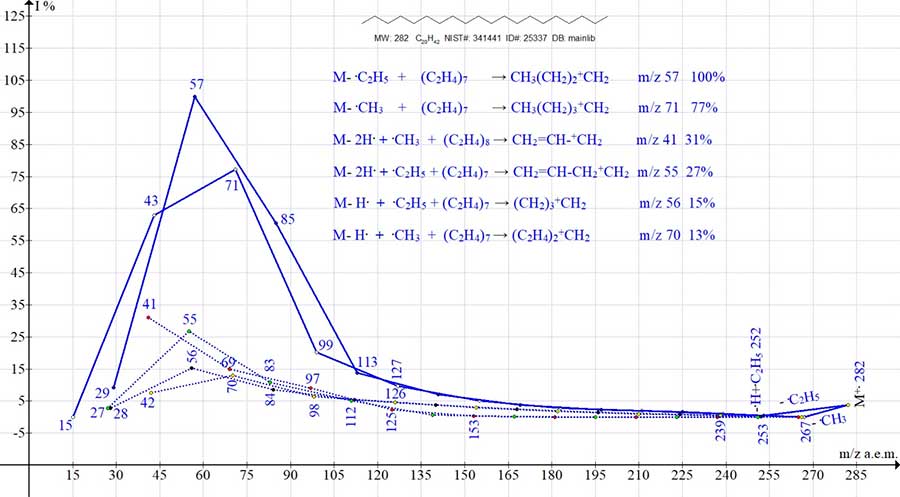
ID#: 25337 DB: mainlib. Две главных алкильных серии отмечены сплошными линиями.
Четыре менее интенсивные серии отмечены пунктирными линиями.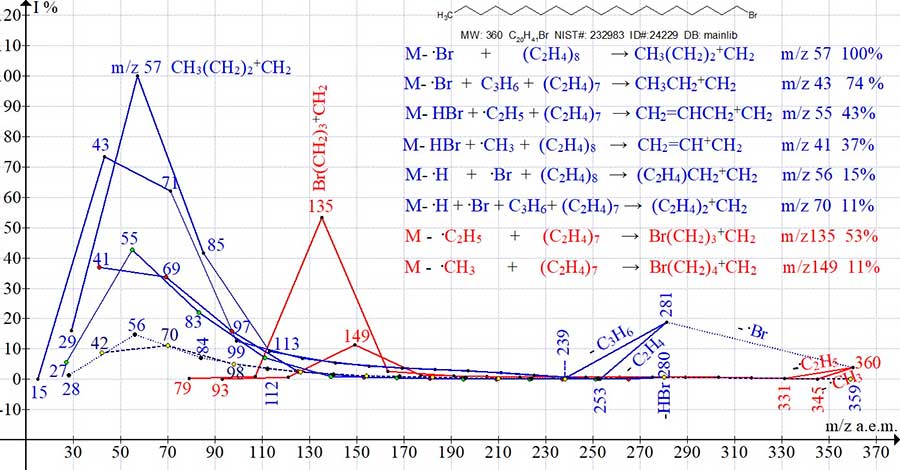
NIST#: 232983 ID#: 24229 DB: mainlib.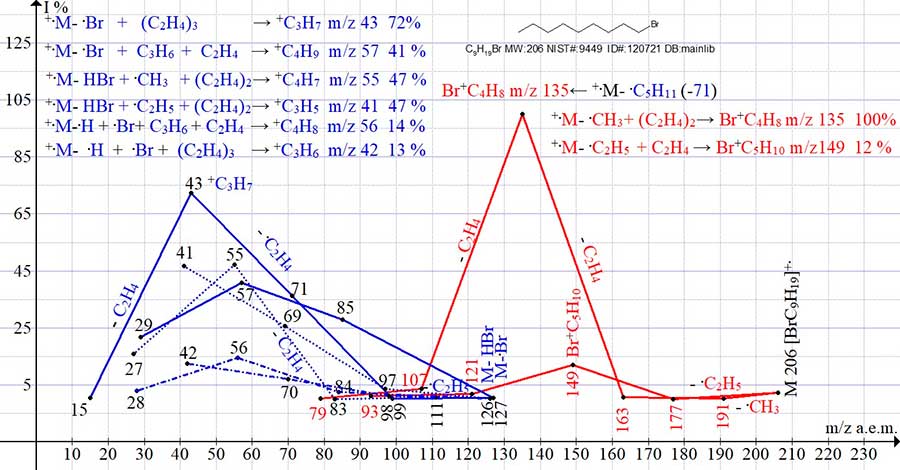
NIST#: 9449 ID#: 120721 DB: mainlib.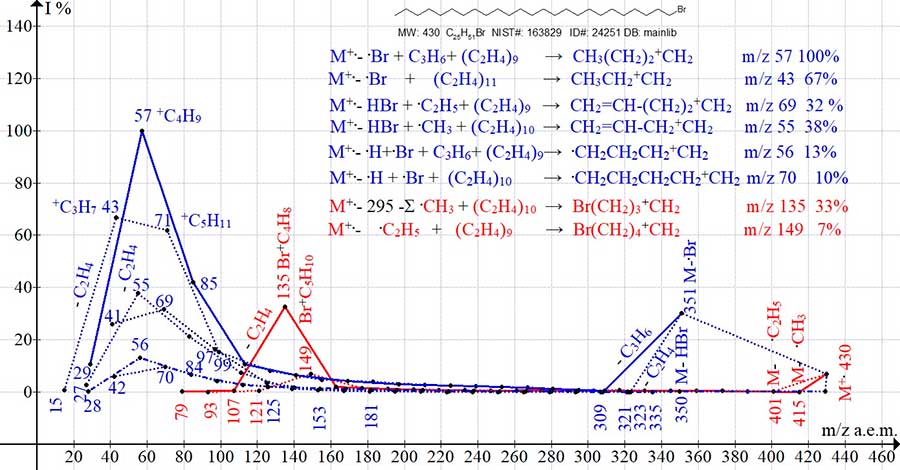
NIST#: 163829 ID#: 24251 DB: mainlib.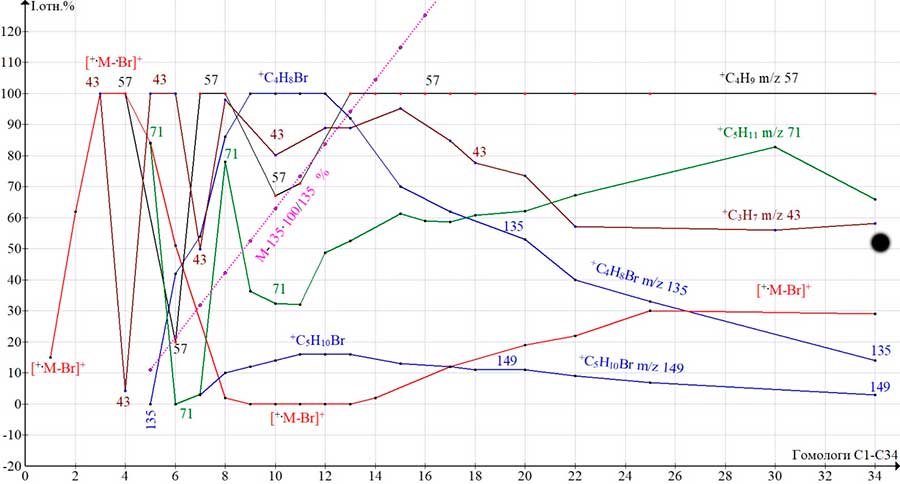
от молекулярной массы гомологов (C1-C34).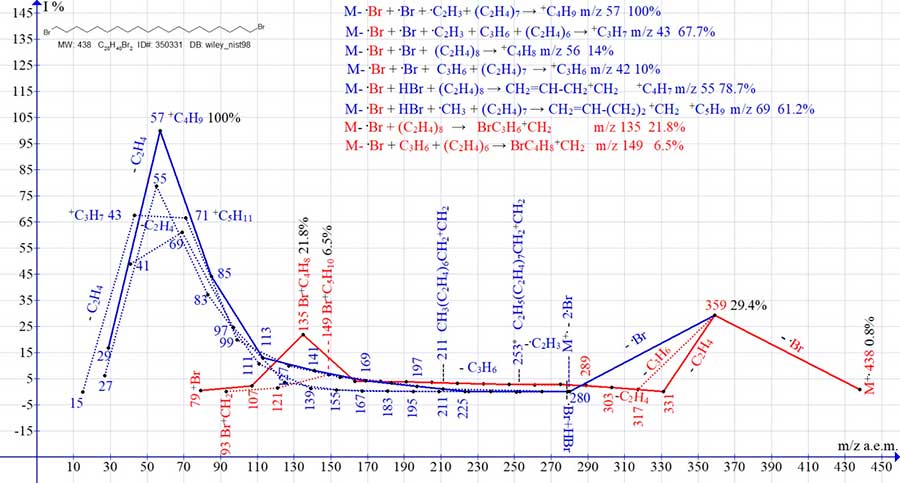
NIST#: 163838 ID#: 24717 DB: mainlib.
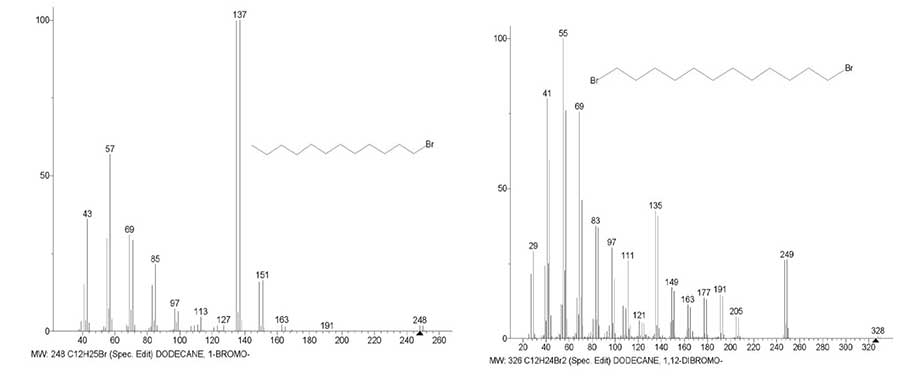
и 1,12-дибром додекана C12H24Br2 MW:326 ID#: 276501 DB: wiley_nist 98.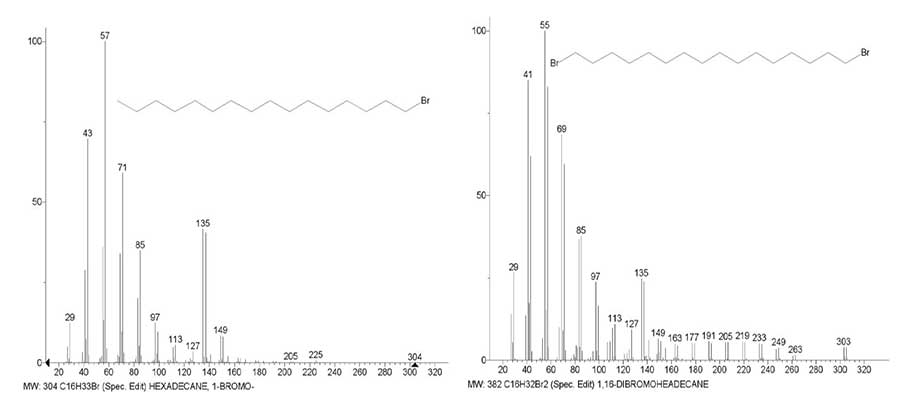
DB: mainlib и 1,16-дибром гексадекана C16H32Br2 MW:382 NIST#: 133768 ID#: 19147
DB:mainlib
ID#: 36291 DB: mainlib и 1,4-дибром октафторбутана C4Br2F8 MW:358 Polaris Q.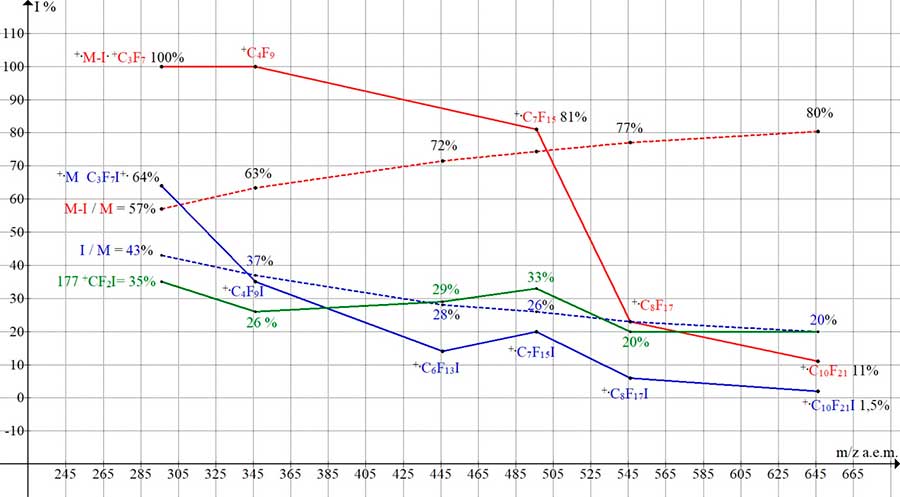
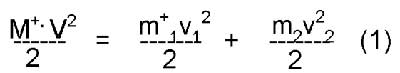

1-бром пентакозана C25H51Br MW: 430 NIST#: 163829 ID#: 24251 DB: mainlib.
(+ график образования иона +C4H8Br красного и иона +C4H9 синего цвета) и две серии их фиктивных интенсивностей этилена (- пунктирные графики красного и синего цвета).Заключение
Благодарности
Список литературы
Fluorine Notes, 2022, 140, 5-6


