Поступило в редакцию: Август 2020
УДК 615.281: 544.18
Fluorine Notes, 2020, 132, 5-6
ТЕОРЕТИЧЕСКАЯ ОЦЕНКА КИСЛОТНОЙ СИЛЫ ПРОТИВОВИРУСНОГО ПРЕПАРАТА ФАВИПИРАВИРА
1 В.А. Бабкин, 1 Д. С. Андреев, 1Ю.А. Вашута, 1А.В. Кожухова,2 В.С. Белоусова, 3,4 Е.С. Титова, 4А.Р. Титова,3А.И. Рахимов,1 А.К. Брель4, Р.О. Болдырев, 5 М.И. Арцис, 5Г.Е. Заиков
1Себряковский филиал Волгоградского государственного технического университета, 403343 Волгоградская область, Михайловка, ул. Мичурина, 2.
e-mail: babkin_v.a@mail.ru
2Первый Московский государственный медицинский университет, имени И.М. Сеченова, 119991, ул. Трубецкая, 8, корпус 2.
e-mail: desdemosha@mail.ru
3Волгоградский государственный технический университет,
400005, Волгоград, проспект Ленина, 28.
e-mail: organic@vstu.ru
4Волгоградский государственный медицинский университет,
400131, Волгоград, пл. Павших Борцов, 1.
e-mail: titova051@rambler.ru
5Институт биохимической физики им. Н.М. Эмануэля РАН,
119334, Москва, ул. Косыгина, д. 4.
e-mail: chembio@sky.chph.ras.ru
Аннотация: Методами AB INITIO и DFT выполнен квантово-химический расчёт противовирусного препарата фавипиравира. Теоретически оценена его кислотная сила (pKa = 13-14, pKa – универсальный показатель кислотности). Установлено, что препарат относится к классу слабых кислот (9 < pKa <14). Высказано предположение, что уменьшение кислотной силы фавипиравира может способствовать повышению его эффективности.
Ключевые слова: фавипиравир, кислотная сила, квантово-химический расчёт, метод AB INITIO, метод DFT, pKa.
Введение
Фавипиравир (6-фторо-3-гидроксипиразин-2-карбоксамид, C5H4FN3O2) – противовирусный препарат, разработанный в Японии для лечения вирусных заболеваний, включая вирусы гриппа, риновирус, респираторно-синцитиальный вирус, а также другие опасные для жизни человека вирусы [1]. Принцип действия основан на ингибировании удлинения формирующейся цепи РНК [2]. В настоящее время фавипиравир изучается как потенциальное средство лечения и других вирусных инфекций, в том числе коронавирусной инфекции COVID-19 [3]. Поэтому вопрос повышения эффективности этого препарата в настоящее время остаётся открытым. Одним из направлений повышения эффективности, как нам представляется, фавипиравира (да и любого медицинского препарата) является возможность управления кислотной силой этого препарата в соответствии с общеизвестным правилом: при уменьшении кислотной силы химического соединения увеличивается его селективность действия до определённой границы, сохраняя его достаточно высокую активность [4].
В связи с этим, целью настоящей работы является теоретическая оценка кислотной силы изучаемого соединения 6-фторо-3-гидроксипиразин-2-карбоксамид путем квантово-химического расчёта его оптимального геометрического и электронного строения и получения различных квантово-химических параметров (общая энергия молекулярной системы C5H4FN3O2 (EО), электронная энергия (Еэл), распределение электронной плотности на атомах – qA, qmaxH+ – максимальный заряд на атоме водорода и т.п.). Данные параметры могут быть использованы и в других исследованиях, например, при изучении механизмов химических и биохимических реакций, в которых может участвовать фавипиравир.
Методическая часть
Для квантово-химического расчёта изучаемого препарата фавипиравира были выбраны два метода AB INITIO/6-311G* и DFT-PBEO/6-311G**. Расчёт выполнялся по программам [5-7], аналогично [8]. Выбор методов обоснован тем, что они являются в настоящее время одними из лучших достаточно хорошо и с высокой точностью воспроизводящими как энергетические характеристики, так и распределение электронной плотности на атомах. Расчёты выполнялись в рамках молекулярной модели [9-10] в газовой фазе.
Результаты расчетов
Оптимизированное геометрическое и электронное строение молекулы фавипиравира показано на рис.1, 2. Квантово-химические параметры (Е0, Еел, qmaxH+) и рКа исследуемого фавипиравира представлены в Таблице 1. Для модели фавипиравира, полученной методом AB INITIO, оптимизированные длины связей между атомами углерода в кольце находятся в диапазоне 1.38-1.51 Å, С-О-1.19-1.32 Å,С-Н-1.07 Å, C-N-1.29-1.35 Å, F-C-1.32 Å, H-N-0.99 Å, H-O-0.94 Å. Оптимизированные значения валентных углов (в градусах) получены соответственно следующие: N(6)-C(2)-C(1)-119,C(5)-N(6)-C(2)-119, C(2)-C(1)-N(3)-121, C(1)-N(3)-C(4)- 119,N(3)-C(4)-C(5)-120, C(4)-C(5)-N(6)-122, C(4)-C(5)-F(7)-120, C(2)-C(1)-O(8)- 122, N(6)-C(2)-C(9)-117, C(1)-C(2)-C(9)-124, C(2)-C(9)-N(10)-114, O(11)-C(9)-N(10)-124, C(2)-C(9)-O(11)-122, N(3)-C(4)-H(12)-119, C(1)-O(8)-H(13)-108, C(9)-N(10)-H(14)-122, C(9)-N(10)-H(15)-118. Заряды на атомах: C(1)-(0.511), C(2)-(-0.033), N(3)-(-0.394), C(4)-(0.03), C(5)-(0.418), N(6)-(-0.378), F(7)-(-0.283), O(8)-(-0.378), C(9)-(0.579), N(10)-(-0.527), O(11)-(-0.458), H(12)-(0.143), H(13)-(0.265), H(14)-(0.261), H(15)-(0.245), (Рис. 1).
Для модели фавипиравира, полученной методом DFT, оптимизированные длины связей между атомами углерода в кольце находится в диапазоне 1.39-1.51 Å, С-О-1.21-1.33 Å, С-Н-1.09 Å, C-N-1.30-1.35 Å, F-C-1.33 Å, H-N-1.00-1.01 Å, H-O-0.97 Å. Оптимизированные значения валентных углов (в градусах) получены соответственно следующие: N(6)-C(2)-C(1)- 119,C(5)-N(6)-C(2)- 119, C(2)-C(1)-N(3)- 121, C(1)-N(3)-C(4)- 119, N(3)-C(4)-C(5)- 120, C(4)-C(5)-N(6)- 123, C(4)-C(5)-F(7)- 120, C(2)-C(1)-O(8)- 122, N(6)-C(2)-C(9)- 117, C(1)-C(2)-C(9)- 124, C(2)-C(9)-N(10)- 113, O(11)-C(9)-N(10)- 124, C(2)-C(9)-O(11)- 123, N(3)-C(4)-H(12)- 119, C(1)-O(8)-H(13)- 106, C(9)-N(10)-H(14)- 120, C(9)-N(10)-H(15)-118.
Заряды на атомах: C(1)-(0.416),C(2)-(-0.033), N(3)-(-0.347), C(4)-(-0.014),C(5)-(0.337), N(6)-(-0.357),F(7)-(-0.207), O(8)-(-0.294), C(9)-(0.439), N(10)-(-0.466), O(11)-(-0.361), H(12)-(0.148), H(13)-(0.249), H(14)-(0.25), H(15)-(0.24) (Рис. 2).
Используя формулу рКа = 49.04 - 134.61qmaxH+ [11], полученную авторами для AB INITIO/6-311G** (qmaxH+ = +0,265), находим значение pKa = 13.
Для метода DFT-PBE0/6-311G** показатель кислотности рассчитывается по формуле: рКа = 51.048-150.078qmaxH+ [7] (qmaxH+ = +0,25). Рассчитанное значение pKa = 14.
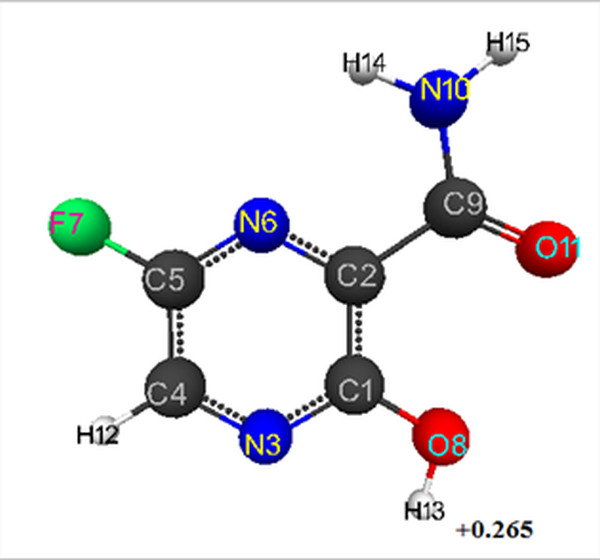
Рисунок 1. Геометрическое и электронное строение молекулы фавипиравира, полученное методом AB INITIO.
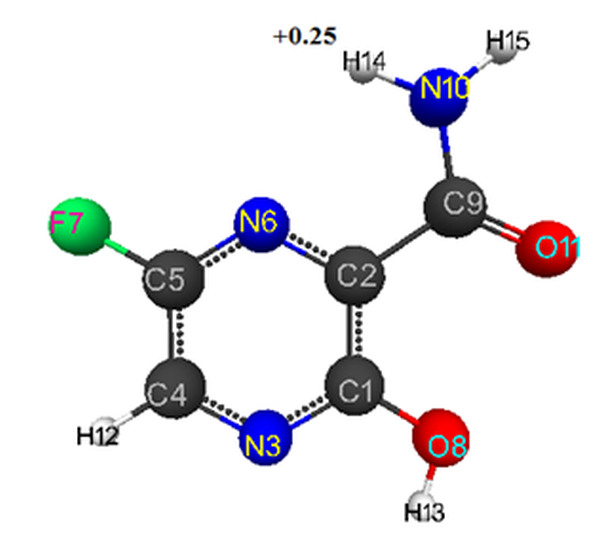
Рисунок 2. Геометрическое и электронное строение молекулы фавипиравира, полученное методом DFT.
Таблица 1. Квантово-химические параметры (Е0, Еэл, qmaxH+) и рКа исследуемого фавипиравира.
|
Препарат |
Метод |
Е0, кДж/моль |
Еел, кДж/моль |
qmaxH+ |
pKa |
|
Фавипиравир |
AB INITIO |
-1586398 |
-3182282 |
+0,265 |
13 |
|
DFT |
-1593396 |
-3178870 |
+0,25 |
14 |
Таким образом, получены оптимизированные атомно-молекулярные структуры изучаемого фавипиравира методами DFT и AB INITIO. Рассчитаны, квантово-химические параметры (Е0, Еэл, qmaxH+), дипольные моменты, распределение электронной плотности на атомах. Доказано, что исследуемый фавипиравир относятся к классу слабых кислот (9<pKa≤14). Очевидно, что предложенная гипотеза зависимости эффективности фавипиравира от его кислотной силы требует экспериментальной верификации.
Список литературы
- Fevipiravis. Dug Information Portal. U.S. National Library at Medicine.
- Aвифавир. Справочник лекарственных препаратов. Medum.ru. 2016, 512 с.
- ru.wikipedia.org. Фавипиравир [электронный ресурс].
- Квантовохимические аспекты катионной полимеризации олефинов, В.А. Бабкин и др., , Издательство "Гилем" (Уфа), 1996, 188 с.
- Granovsky, A. A., Firefly version 8, 2013. http://classic.chem.msu.su/gran/firefly/index.html
- MacMolPlt: A Graphical User Interface for GAMESS., B.M. Bode, M.S. Gordon, Journal of Molecular Graphics, 1998, 16, 133-138.
- General Atomic and Molecular Electronic Structure System, M.W. Schmidt [and others], J.Comput.Chem. 1993, 14, 1347-1363.
- Quantum-Chemical Calculation of Some Molecules of Triftoromethylstyroles by the DFT Method. V.А. Babkin and others, Fluorine Notes, 2019, 123, 5-6
- Ермаков А.Т. Квантовая механика и квантовая химия, Изд-во Юрайт, 2016, 555 с.
- Цирельсон, В.Г., Квантовая химия. Молекулы, молекулярные системы и твердые тела. Изд-во Бином, 2010, 422 с.
- Connection of the universal acidity index of H-acid with the charge on Hydrogen atom (AB INITIO method). V. A. Babkin and others, Oxidation Communications, 2002, 25(1), 21-47.
Статья рекомендована к публикации членом редколлегии д.х.н. С.М. Игумновым
Fluorine Notes, 2020, 132, 5-6


