Поступило в редакцию: Октябрь 2020
УДК 543.51+547
Fluorine Notes, 2020, 132, 3-4
НОВЫЙ ВЗГЛЯД НА ПЕРЕГРУППИРОВКУ МАК-ЛАФФЕРТИ В СПЕКТРАХ н-КАРБОНОВЫХ КИСЛОТ ИХ МЕТИЛОВЫХ И 2,2,2-ТРИФТОРЭТИЛОВЫХ ЭФИРОВ
Н.Д. Каграманов
Институт элементоорганических соединений им. А. Н. Несмеянова Российской академии наук, 119991, ГСП-1, Москва, В-334, ул. Вавилова, д. 28
e-mail: ndkagram@gmail.com
Аннотация: Причиной, стимулировавшей интерес к данной теме, стала проверка алгоритма, предложенного для фрагментации н-алканов, в условиях перегруппировочных процессов, происходящих в спектрах н-карбоновых кислот их метиловых эфиров и 2,2,2- трифторэтиловых эфиров, представленных в библиотеках NIST. Анализом спектров гомологов кислот С5-С34, метиловых С5-С61 и трифторэтиловых эфиров C6-C22, подтверждено, что фрагментация их алкильной цепи, происходит без перегруппировок вплоть до иона [C4H7O2]+ с m/z 87 в спектрах кислот, ионов [C5H9O2]+ с m/z 101 и [C6H8F3O2]+ с m/z 169 в спектрах метиловых и трифторэтиловых эфиров. В отличие от предшествующих отрывов, отрыв этилена от ионов с m/z 87, m/z 101 и m/z 169 сопровождается возникновением двух ионов: перегруппировочного, и c потерей атома водорода, более стабильного, фрагментного перегруппировочного иона. Перегруппировочные ионы с m/z 61, 75 и 143 возникают из ионов 87, 101 и 169, в результате координационных взаимодействий кислорода карбонильной группы с двумя атомами водорода концевой этиленовой группы, распада переходного состояния с выбросом ацетилена и присоединением к новому иону двух атомов водорода. В спектрах карбоновых кислот С5-С30 их метиловых и трифторэтиловых эфиров образуются пары ионов: CH2=C(HO+Н)(OH) c m/z 61 и .CH2C=(O+H)(OH) c m/z 60; CH2=C(HO+Н)(OСH3) c m/z 75 и CH2C=(O+H)(OCH3) c m/z 74; CH2=C(HO+H)(OCH2CF3) c m/z 143 и .CH2C=(O+H)(OCH2CF3) c m/z 142. Соотношение интенсивностей пиков перегруппировочных и фрагментных перегруппировочных ионов с m/z 61 и 60; 75 и 74; 143 и142 возрастает при увеличении молекулярной массы гомолога, в результате снижения колебательного возбуждения M+..
Ключевые слова: перегруппировка Мак-Лафферти, масс-спектрометрия карбоновых кислот, серии ионов.
Введение
Впервые о внутримолекулярных перегруппировках, происходящих при фотолизе диалкилкетонов: n-AmCOMe, sec-BuCOMe и n-PrCOMe с образованием смесей: ацетона и 1-бутена, EtCOMe и этилена, ацетона и этилена соответственно сообщалось в работе Никольсона А.Дж.С. [1].
Перегруппировка, известная как перегруппировка Мак-Лафферти, была обнаружена Фредом Уорреном Мак-Лафферти в масс-спектрах алифатических кетонов, карбоновых кислот, эфиров кислот и широкого круга соединений, содержащих ненасыщенные группы C=O, C=N, C=C, C=S, обладающих сильными электроноакцепторными свойствами [2]. В спектрах карбонильных соединений перегруппировка региоселективна. Её возможность зависит от наличия в цепи не менее трех последовательно соединенных групп CH2, наличия в γ-положении, по отношению к кислороду карбонильной группы атома H, причем расстояние между атомами не должно превышать 0,18нм [3]. В масс-спектре н-бутановой кислоты C3H7‑COOH перегруппировка молекулярного иона происходит с отрывом этилена, через шестичленное переходное состояние (Рис.1) [2].
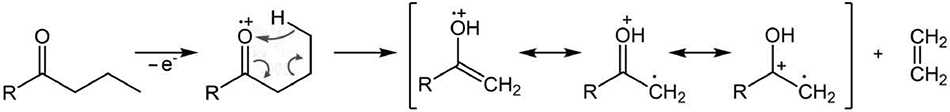
Рисунок 1. Cxема перегруппировки Мак-Лафферти (R=OH, OCH3).
Подтверждением перегруппировки является характерный базовый ион
.CH2C=(O+H)(HO) c m/z 60, отличающийся от "ожидаемого" иона
+.M – . C2H5 -> +CH2 C=O(HO) с m/z 59.
В спектрах С5, валериановой и изовалериановой кислот, наряду с интенсивным пиком с m/z 60 образуется заметный пик двойной перегруппировки - двух атомов водорода, с m/z 61 [4,2]. Двойная перегруппировка отличается от перегруппировки одного атома водорода, тем, что вместо молекулы образуется радикал [2]. Если в перегруппировке бутановой кислоты с миграцией одного атома H и отрывом этилена участвует молекулярный ион, то в случае высших карбоновых кислот возникает неопределенность, от какого из углеродных атомов происходит отрыв одного или двух атома водорода и какой олефин при этом образуется. Отрывается ли водород, также как в бутановой кислоте, через шестичленное переходное состояние, или это происходит по механизму, включающему миграцию H-атомов из более далеких положений путем сдвига к карбонилу. Был сделан ряд предположений о возникновении перегруппировочных ионов, массы которых соответствуют обычным ожидаемым ионам, но пики имеют повышенную интенсивность, указывающую на их высокую стабильность и, следовательно, возможность внутримолекулярной перегруппировки без изменения массы. «Начиная с нормальных кислот состава C10 в спектрах появляются гомологические ионы с m/z 129 CH2=CH-(CH2)3-C=O+H(OH), которые, как и ионы RCH=CR1-C=O+H(OH), возможно, являются следствием первоначального сдвига одного и того же атома водорода» [5]. Образование ионов, имеющих повышенную интенсивность, объяснялось неспецифическими миграциями водорода (тип Р), через переходные состояния, когда размер цикла переходного состояния не определен и не имеет существенного значения [6]. «В масс-спектрах метиловых эфиров длинноцепочечных карбоновых кислот R(CH2)nCOOCH3 (n>5) наблюдаются интенсивные пики ионов-гомологов +(СH2)nCOOCH3. Наиболее интенсивный пик (>50%) дает ион с m/e 87 (n=2). Структура +CH2CH2COOCH3 никак не может объяснить столь высокой интенсивности. Было показано, что ион m/e 87, получается, по представленному ниже механизму путем первоначальной дальней миграции H-атома к карбонильной группе, последующей обратной миграции подвижного атома водорода из α-положения по отношению к карбометоксильной группе к образовавшемуся радикальному центру и, наконец, путем разрыва связи по типу Б1 (или А2): (представлена схема). Ион с m/e 87 +CH2CH=C(OH)OCH3, безусловно, стабильнее иона +CH2CH2COOCH3» [6].
Сходная аргументация высокой интенсивности пиков ионов-гомологов, в спектрах метиловых эфиров карбоновых кислот (через каждые четыре метиленовых звена), схема образования (8.67а) и структура иона с m/z 87 СН2=CH-C=O+H(OCH3) представлены в монографии [7]. В отношении фрагментации н-карбоновых кислот в этом же обзоре, на стр.261, автор отмечает: «Чем длиннее алкильная цепь, тем выше интенсивность пика иона с m/z 61, образующегося при миграции к карбоксильной группе двух атомов водорода алкильной цепи» [7].
Обсуждаемые в настоящем сообщении вероятные схемы образования перегруппировочных ионов, а также причины повышенной интенсивности ионов-гомологов рассмотрены, исходя из подробного анализа спектров карбоновых кислот, их метиловых эфиров и 2,2,2-трифторэтиловых эфиров, выполненного, согласно алгоритму фрагментации н-алканов [8].
Фрагментация гомологов С4-С34 н-карбоновых кислот
Анализом спектров н-алканов установлено, что их спектр является суммой двух главных, параллельно образующихся серий ионов, начинающихся с отрывов метильного и этильного радикалов и последующих выбросов молекул этилена [8]. В Табл. 1 представлены: информативная часть спектра н-пентадекановой кислоты (NIST Library), а так же эмулированные по алгоритму н-алканов массовые числа ее спектра при отрывах .CH3 и .C2H5. Эмуляция спектра выполнена с целью подтверждения, что реальный спектр н-пентадекановой кислоты действительно представляет собой сумму двух, независимых серий ионов, позволяющих различить серию, в которой происходит перегруппировка с образованием ионов с m/z 61 и 60 и серию, в которой эти ионы не образуются.
Таблица 1. Табличный масс-спектр н-пентадекановой кислоты C15H30O2 и массовые числа ее эмулированного спектра.
Масс-спектр CH3[CH2]14COOH [NIST Library]
|
45 11,6% |
60 93,1% |
61 22,8% |
73 100% |
87 21,8% |
101 9,7% |
115 14,5% |
129 44,1% |
143 16,4% |
157 9,2% |
171 8,1% |
185 12,2% |
199 18,6% |
213 3,7% |
227 0,1% |
242 15,9% М |
Массовые числа спектра н-C15H30O2,эмулированного при первичном отрыве ·CH3.
|
-1 |
-26 |
-28 |
-28 |
-28 |
-28 |
-28 |
-15 |
Масса |
|
- H |
- HCCH |
- H2C=CH2 |
- H2C=CH2 |
- H2C=CH2 |
- H2C=CH2 |
- H2C=CH2 |
. CH3 |
242 |
|
60 |
61 |
87 |
115 |
143 |
171 |
199 |
227 |
m/z |
Массовые числа спектра н-C15H30O2, эмулированного при первичном отрыве ·C2H5
|
-28 |
-28 |
-28 |
-28 |
-28 |
-28 |
-29 |
Масса |
|
- H2C=CH2 |
- H2C=CH2 |
- H2C=CH2 |
- H2C=CH2 |
- H2C=H2C |
- CH2=CH2 |
. H2C-CH3 |
242 |
|
45 |
73 |
101 |
129 |
157 |
185 |
213 |
m/z |
Массовые числа спектра н-пентадекановой кислоты, эмулированного при отрывах CH3 и·C2H5.
|
45 |
60 |
61 |
73 |
87 |
101 |
115 |
129 |
143 |
157 |
171 |
185 |
199 |
213 |
227 |
242 |
Сравнение масс-спектра н-пентадекановой кислоты с массовыми числами ее спектра, эмулированного по алгоритму параллельных первичных отрывов ·CH3 и ·C2H5 с последующими выбросами этилена (Табл. 1.) подтверждает их полное совпадение и образование перегруппировочных ионов с m/z 61и 60 только в одной из серий.
Представленные на Рис. 2 графики интенсивностей основных пиков масс-спектров гомологов C2-C30 н-карбоновых кислот иллюстрируют их зависимость от молекулярной массы 60-452 Да.
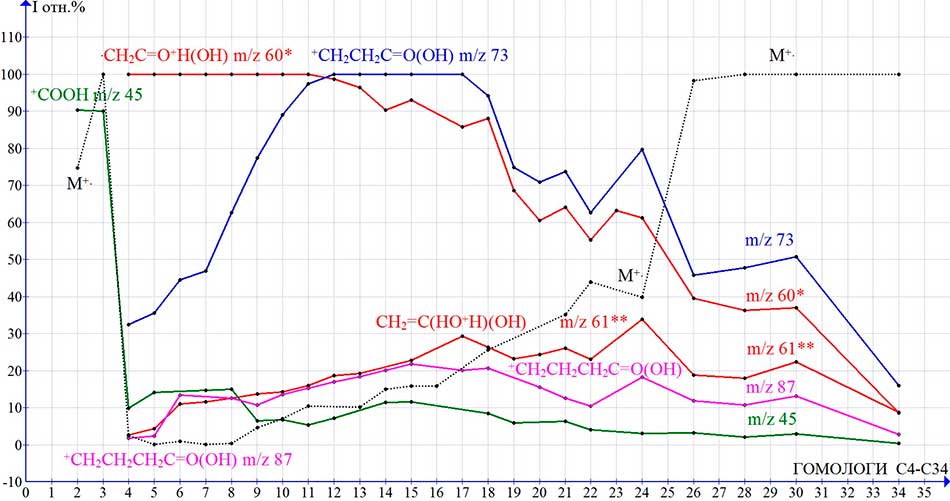
Рисунок 2. Зависимости интенсивностей (I отн.%) пиков ионов н-карбоновых кислот от их молекулярной массы.
Высокие интенсивности M+. C2-С3 75 и 100%, не связаны с перегруппировкой, а так же, как базовый молекулярный пик C1 н-алканов, M+. C1-С2 н-алкилхлоридов и н-алкилбромидов [8,9] результат прочности структур первых гомологов и минимальной возможности фрагментации, по сравнению со структурами следующих гомологов и возможностями их фрагментаций. Причиной высокой интенсивности M+. пиков кислот C2-С3 является оптимальные соотношения масс их акильной цепи и гидроксикарбонильной группы 1:3 и 1:1,6. Начиная с C9, происходит рост интенсивности M+. в результате снижения колебательного возбуждения при увеличении молекулярной массы. Падение интенсивности пиков фрагментных ионов гомологов C17-C34 вероятно результат увеличения дефицита энергии, необходимой для полноценной фрагментации M+..
Перегруппировка бутановой кислоты С4 происходит через шестичленное переходное состояние молекулярного катион-радикала (Рис. 1) с миграцией одного атома водорода C2H5 группы к кислороду карбонила и выбросом молекулы этилена [2]. Наряду с базовым перегруппировочным ионом с m/z 60, в спектре присутствует ион с m/z 61 интенсивность пика которого 2,6 %, соответствует интенсивности изотопного пика C13 2,36%. Еще одним процессом распада M+. C4 является отрыв . CH3, происходящий в неперегруппировочной серии, c образованием иона +CH2CH2C=O(OH) m/z 73 32,4%, фрагментирующего с выбросом С2H4 и образованием иона +COOH. C увеличением молекулярной массы, в спектрах гомологов С11-С17 пик 73 становится базовым, а в спектрах C18-C34 интенсивность его начинает снижаться так же, как интенсивность перегруппировочного пика с m/z 60 (Рис. 2). Высокая интенсивность пика иона с m/z 73 позволяла предполагать, что либо структура его не соответствует +CH2CH2C=O(OH) и за счет сдвига атома водорода ион перегруппировывается в CH2=CH-C=O+H(OH), либо существует другая, альтернативная причина его высокой интенсивности.
У гомолога C5 интенсивность пика с m/z 61 4,4%, что в два раза больше интенсивности изотопного пика C13, а у гомолога C11 она уже 16%. В спектрах C5-С34 перегруппировочный ион с m/z 61 образуется из фрагментного иона c m/z 87 через переходное состояние с миграцией двух атомов водорода концевой этиленовой группы к карбонильному кислороду с выбросом молекулы ацетилена (Рис. 3).
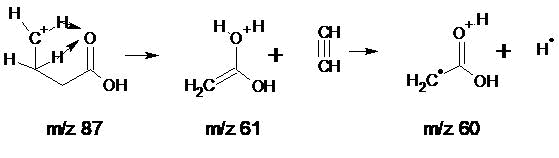
Рисунок 3. Схема образования перегруппировочного иона: С2H5O2 c m/z 61 и его фрагментного перегруппировочного иона С2H4O2 c m/z 60.
Энергии отрыва этилена, ацетилена, винильного радикала и атомов H от концевой этиленовой группы иона с m/z 87, можно приближенно оценить, сравнив значения стандартных энтальпий образования отрываемых фрагментов (Таблица 2).
В спектре C5, прямое превращение иона с m/z 87 в перегруппировочный ион с m/z 60 возможно при миграции к кислороду карбонила одного атома водорода концевой этиленовой группы, с отрывом винильного радикала ΔHf0 = 70,5ккал/моль.
В масс-спектрах н-алканов одним из наиболее энергозатратных процессов является отрыв атомов водорода, энтальпия образования которого составляет ΔHf0 = 52,1ккал/моль.
Таблица 2. Энтальпии образования ΔHf0 [10*].
|
CH2=HC. |
C2H2 |
.H |
C2H4 |
C3H6 |
C4H8 |
|
|
ΔHf0 (г), 298K (ккал/моль) |
70,5* |
54,2 (спр.) |
52,1* |
12,5 (спр.) |
4,88 (спр.) |
-0,03 (спр.) |
Для отрыва от этилена двух атомов водорода с образованием ацетилена необходимо затратить 54,2 ккал/моль, что почти совпадает с энтальпией образования атома водорода 52,1 ккал/моль. По сравнению с энтальпией этилена, заслуживает внимание минимальная величина энтальпии образования С4H8.
Меняющееся при увеличении молекулярной массы гомологов соотношение интенсивностей пиков ионов с m/z 61 и 60, позволяет заключить, что прочности связей двух атомов водорода, координированных карбонильной группой, различаются. Ион с m/z 61 CH2=C-O+H2(OH), образующийся при отрыве ацетилена от иона +(CH2)3COOH, менее стабилен, чем его фрагментный ион с m/z 60 .CH2C=O+H(OH). Однако с увеличением молекулярной массы и снижением избыточного возбуждения интенсивность пика с m/z 61 увеличивается, и в спектре С34 интенсивности пиков с m/z 61 и 60 одинаковы.
На Рис.4 представлен масс-спектр пентадекановой кислоты и график двух главных серий ионов, с реальными интенсивностями пиков.

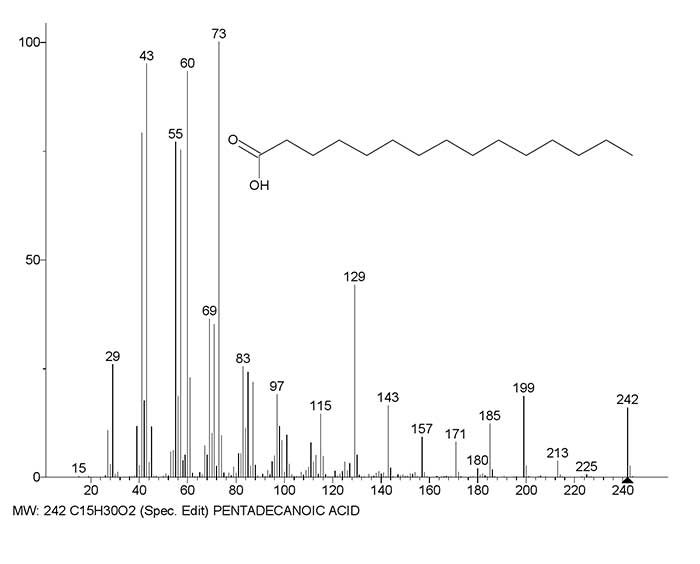
Рисунок 4. Масс-спектр пентадекановой кислоты C15H30O2 и график двух серий ионов спектра с реальными интенсивностями пиков.
В серии, приводящей к перегруппировочным ионам с m/z 61 и 60 ( Рис.4 сер. красного цвета), все предшествующие пики: 199, 171, 143, 115, 87, различающиеся на этиленовые группы, имеют близкую интенсивность, порядка 20%. В серии, приводящей к иону с m/z 73 (Рис.4 сер. синего цвета), пики c m/z 185, 129 и 73, различающиеся на бутиленовые группы, имеют более высокие интенсивности 12, 44 и 100%.
С ростом молекулярной массы гомологов, число интенсивных пиков, различающихся на группу C4H8, увеличивается. В спектре C22 таких ионов пять: 297, 241,185,129 и 73. Исходя из повышенной интенсивности пиков, нет основания предполагать, что эти пять ионов являются перегруппировочными.
По сравнению с отрывами C2H4, отрыв С4H8 приводит к удвоенному отводу избыточной энергии, а увеличение числа таких отрывов способствует большей стабилизация образующихся ионов и росту интенсивности их пиков. То есть, наряду с «медленной» (отрывы C2H4) перегруппировочной серией (Рис.4 сер. красного цвета) образуется «быстрая» (отрывы С4H8) неперегруппировочная серия (Рис.4 сер. синего цвета).
Фрагментация гомологов кислот с третичным атомом углерода в положении 3 (Рис. 5,6) происходит так же, как в спектрах н-карбоновых кислот с отрывом ацетилена и образованием двух перегруппировочных ионов с m/z 61 и 60. Однако в кислотах с третичным атомом углерода и двумя алкильными цепями число возможных отрывов С4H8 меньше, чем в н-карбоновых кислотах с тем же числом углеродных атомов, что вероятно является причиной снижения интенсивности пика с m/z 73.
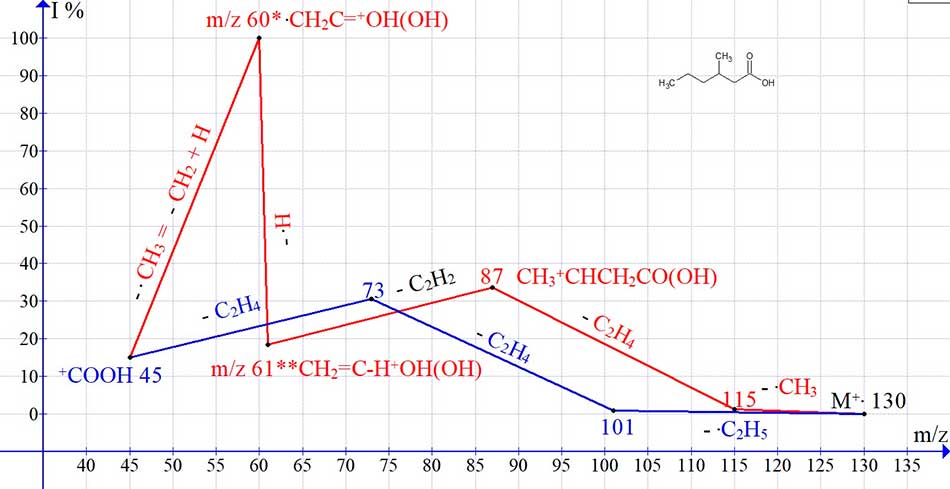
Рисунок 5. График двух серий ионов спектра C7H14O2, с реальными интенсивностями пиков.
Более сложно происходит фрагментация 3-этилгептановой кислоты (Рис. 6).

Рисунок 6. График двух серий ионов спектра C9H18O2, с реальными интенсивностями пиков.
В спектре С9H18O2 после отрыва (от цепи С4) метильного радикала и молекулы этилена (Рис.6 сер. красного цвета) происходит выброс винильного радикала .СH-CH2, включающий третичный атом углерода. Это приводит к перестройке цепи и дополнительному отрыву атома водорода концевой метильной группы (что в сумме равнозначно отрыву этилена) с образованием иона +СН2СH2CH2COOH с m/z 87. Ион с m/z 87 фрагментирует далее с образованием перегруппировочного иона с m/z 61 и его фрагментного иона с m/z 60.
Перегруппировки гомологов кислот с третичным атомом углерода в положении 2 (на примере С20H40O2) затруднены отсутствием во втором положении стабилизирующей метиленовой группы. Перегруппировочная серия фрагментации С20H40O2 (Рис.7сер. красного цвета) начинается с отрыва радикала .С2H5 от малой цепи С8. В результате двух последующих отрывов C2H4 образуется ион с m/z 227, фрагментирующий с отрывом винильного радикала и миграцией только одного атома водорода к карбонильной группе. Последующий распад перегруппировочного иона с m/z 200* c повторным выбросом винильного радикала из положений 2-3 и атома водорода, то есть молекулы этилена, приводит к иону с m/z 172. Далее происходит отрыв концевой группы .С2H5, последующая этиленовая фрагментация с образованием иона с m/z 87 и отрыв винильного радикала с образованием перегруппировочного иона с m/z 60.
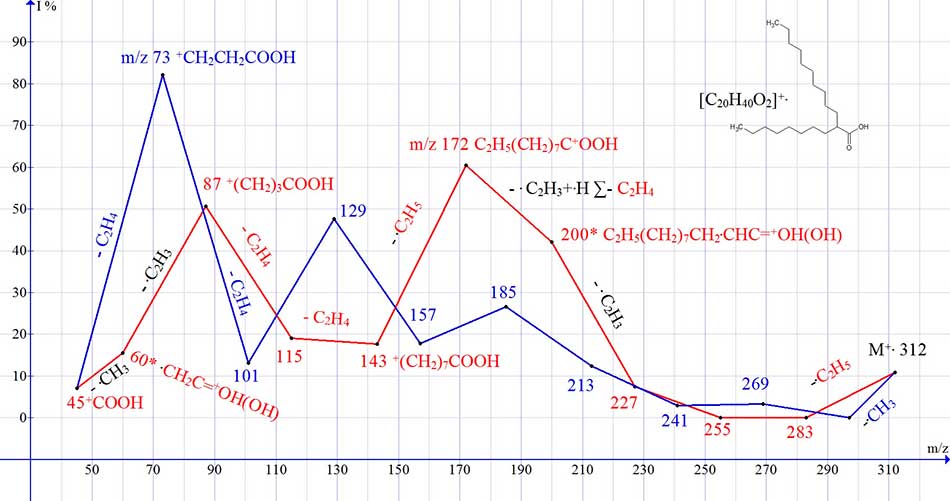
Рисунок 7. График двух серий ионов спектра C20H40O2, с реальными интенсивностями пиков.
В неперегруппировочной серии (Рис. 7 сер. синего цвета) интенсивность пика иона с m/z 73 82%- результат 3-х отрывов С4H8, с образованием возрастающих по интенсивности пиков c m/z 185,129 и 73.
Таким образом, в спектрах карбоновых кислот образуются следующие перегруппировочные ионы:
- фрагментный перегруппировочный ион с m/z 60 .CH2C=(O+H)(OH) бутановой кислоты C4 100%, образуется при отрыве одного атома водорода от этильной группы молекулярного иона CH3CH2CH2CO+.(OH) c выбросом этилена;
- фрагментный перегруппировочный ион с m/z 61 CH2=C(HO+H)(OH) в спектрах гомологов C5-C30 7,4 - 22,0%, образуется при отрывах двух атомов водорода от концевой этиленовой группы фрагментного иона с m/z 87 +CH2CH2CH2COOH с выбросом ацетилена;
- фрагментный перегруппировочный ион с m/z 60 . CH2C=(O+H)(OH) гомологов C5-C30 100‑37%, образуется при отрыве одного атомов водородаот перегруппировочного иона с m/z 61.
При фрагментации 3-этилгептановой кислоты C7 ион с m/z 115, включающий третичный атом углерода, выбрасывает винильный радикал .СH-CH2. Это приводит к перестройке цепи и дополнительному отрыву атома водорода концевой метильной группы (что в сумме равнозначно отрыву этилена) с образованием иона +СН2СH2CH2COOH с m/z 87.
При отрыве от иона с m/z 87 ацетилена возникает перегруппировочный ион с m/z 61 18.5% CH2=C(HO+H)(OH).
Перегруппировки гомологов кислот с третичным атомом углерода в положении 2 (на примере С20H40O2) затруднены отсутствием во втором положении стабилизирующей метиленовой группы. В результате двух отрывов C2H4 образуется ион с m/z 227, фрагментирующий, вместо выброса ацетилена, с отрывом винильного радикала и миграцией только одного атома водорода к карбонильной группе.
Фрагментация гомологов С4-С61 метиловых эфиров н-карбоновых кислот
Перегруппировка Мак-Лафферти в спектре метилового эфира гомолога С5 начинается с отрыва этилена от молекулярного иона CH3CH2CH2CO+.(OCH3) (Рис. 8).
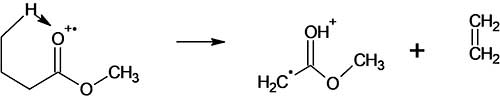
Рисунок 8. Схема образования перегруппировочного иона С3H6O2 c m/z 74.
Если в спектре метилового эфира бутановой кислоты интенсивность пика иона с m/z 75 2.7% соответствует
интенсивности изотопного пика C13, то у гомологов С26-C29 (Рис.
9) она возрастает до 37-48 %. Рост интенсивности пика с m/z 75 подтверждает образование перегруппировочного
иона c двумя координированными атомами водорода СH2=C(HO+H)(OCH3)
в результате выброса ацетилена ионом +CH2CH2CH2COOCH3 с m/z 101.
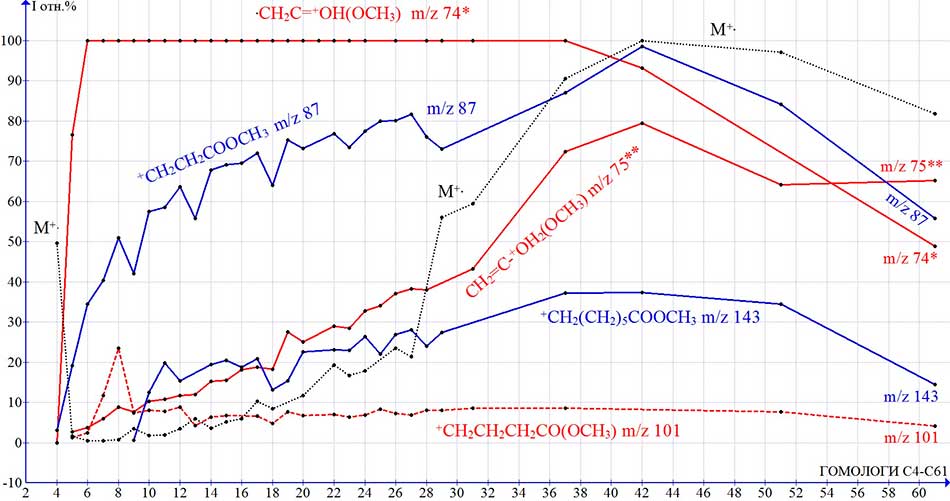
Рисунок 9. Зависимости интенсивностей ( I отн.%) пиков ионов метиловых эфиров н-карбоновых кислот от их молекулярной массы.
При увеличении молекулярной массы гомологов наряду с ростом интенсивности пика перегруппировочного иона с m/z 75 происходит так же рост интенсивности молекулярного иона. Интенсивность пика иона c m/z 101, являющегося материнским ионом перегруппировочного иона с m/z 75 сохраняется постоянной, на уровне 8%.
На Рис. 10 представлен масс-спектр метилового эфира октакозановой кислоты и график двух серий ионов, с реальными интенсивностями пиков.

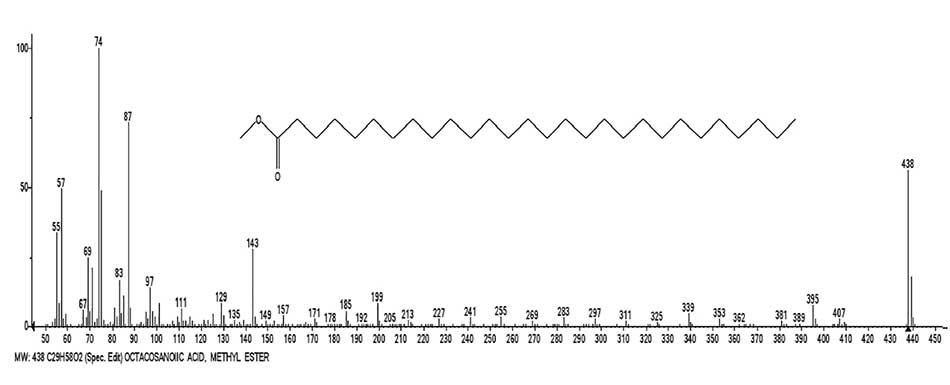
Рисунок 10. Масс-спектр метилового эфира октакозановой кислоты С29H58O2 и график двух серий ионов спектра, с реальными интенсивностями пиков.
Фрагментация метиловых эфиров С5-С61, как и фрагментация н-карбоновых кислот происходит с отрывом ацетилена и образованием перегруппировочного иона с m/z 75 и его фрагментного перегруппировочного иона с m/z 74.
Так же как в спектрах карбоновых кислот, в неперегруппировочной серии спектров метиловых эфиров (Рис.10 сер. синего цвета) происходит образование интенсивных ионов с m/z 87, 199 и 143, различающихся на С4H8 группу.
Фрагментация гомологов С5-С22 2,2,2-трифторэтиловых эфиров н-карбоновых кислот
Зависимости интенсивностей пиков ионов трифторэтиловых эфиров от их молекулярной массы (Рис. 11), отличаются
от аналогичных зависимостей для н-карбоновых кислот (Рис. 2) и их метиловых эфиров (Рис. 9), тем,
что имеют более пологий характер.

Рисунок 11. Зависимости интенсивностей (I отн.%) пиков ионов 2,2,2-трифторэтиловых эфиров н-карбоновых кислот от их молекулярной массы.
Это связано с тем, что с одной стороны диапазон представленных спектров гомологов трифторэтиловых эфиров существенно меньше, чем в случае карбоновых кислот. С другой стороны, поскольку масса трифторэтилового эфира на 82 Да (группу CHCF3) больше массы н-карбоновой кислоты, вероятно, что увеличение масс гомологов на группы CH2 в большей мере скажется на фрагментации н-карбоновых кислот, чем их трифторэтиловых эфиров.
На Рис. 12 представлен масс-спектр 2,2,2-трифторэтилового эфира эйкозановой кислоты и график двух серий ионов спектра, с реальными интенсивностями пиков.

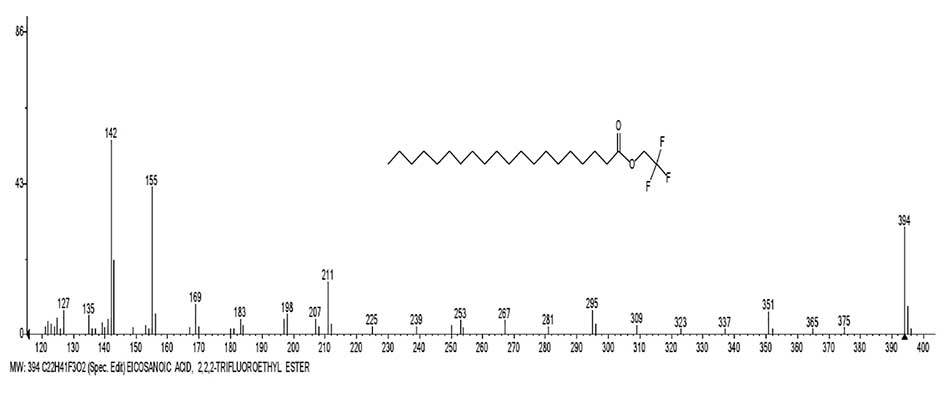
Рисунок 12. Масс-спектр 2,2,2- трифторэтилового эфира эйкозановой кислоты С22H41 F3O2 и график двух серий ионов спектра, с реальными интенсивностями пиков.
В трифторэтиловых эфирах карбоновых кислот группа CF3, обладающая сильным электроноакцепторным свойством, отделена от карбонильной группы метиленовой группой и атомом кислорода, что исключает ее влияние на перегруппировку. В спектрах трифторэтиловых эфиров карбоновых кислот (Рис. 12) перегруппировки происходят такие же, как в спектрах кислот с отрывом ацетилена и образованием перегруппировочного иона с m/z 143 и его фрагментного иона с m/z 142.
В отличие от трифторэтиловых эфиров карбоновых кислот, в эфирах трифторуксусной кислоты группа CF3 смещает на себя электронную плотность углеродного атома карбонильной группы, ослабляя соседнюю связь CF3C=O - OR. Это ослабление связи вероятно и определяет состав перегруппировочного иона СF3HС=HO+ с m/z 99. Отрыва С2H2 от иона СF3C=OOCH2CH+2 c m/z 141 не происходит, так как пик иона СF3C=O+H(OH) с m/z 115 имеет минимальную интенсивность 0.9-0.3%.
На Рис. 13 представлены перегруппировочные процессы фрагментации, происходящие в масс-спектрах гомологов С4, C5 и С9 эфиров трифторуксусной кислоты.
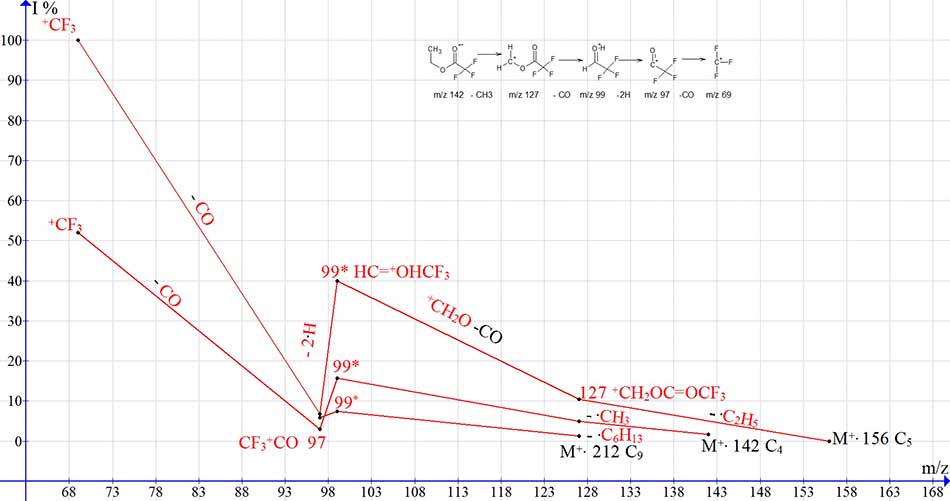
Рисунок 13. Перегруппировочные серии ионов масс-спектров С4,С5 и С9 эфиров трифторуксусной кислоты c реальными интенсивностями пиков.
В масс-спектре гомолога С11H19F3O2 MW 240, масса алкильной цепи С9H19 =127, превышающую массу трифторуксусной кислоты 114, может быть причиной изменения фрагментации – прекращения перегруппировки с образованием ионов с m/z 127 CF3COOCH+2 и c m/z 99 CF3 HC=O+H. В результате спектры гомологов С11-С22 MW 240-394 становятся спектрами олефиновых СnH2n , алкенильных ионов СnH2n-1 и алкильных ионов СnH2n+1.
Выводы
Алгоритмом фрагментации, предложенным для н-алканов, успешно подтверждены последовательности образования и распада перегруппировочных ионов в спектрах гомологов н-карбоновых кислот, кислот с третичным углеродным атомом, метиловых и трифторэтиловых эфиров н-карбоновых кислот.
Ионами, фрагментирующими с перегруппировкой, являются:
- в н-карбоновых кислотах +CH2-CH2-CH2-COOH с m/z 87;
- в метиловых эфирах кислот +CH2-CH2-CH2-COOCH3 с m/z 101;
- в трифторэтиловых эфирах +CH2-CH2-CH2-COOCH2CF3 с m/z 169;
В перегруппировках Мак-Лафферти атом кислорода карбонильной группы координирует два атома водорода концевых этиленовых групп ионов 87, 101 и 169, с выбросом молекулы ацетилена.
В результате образуются два иона: перегруппировочный и более стабильный фрагментный-перегруппировочный ион с потерей одного атома водорода:
- CH2 =C(HO+Н)(OH) c m/z 61 и .CH2 C=(O+H)(OH) c m/z 60;
- CH2 =C(HO+Н)(OСH3) c m/z 75 и .CH2 C=(O+H)(OCH3 ) c m/z 74;
- CH2= C(HO+H)OCH2CF3 c m/z 143 и .CH2 C=(O+H)OCH2CF3 c m/z 142.
Соотношение интенсивностей пиков перегруппировочных и фрагментных ионов с m/z 61 и 60, 75 и 74, 143 и142 возрастает при увеличении молекулярной массы гомолога, в результате снижения колебательного возбуждения M+..
Масс-спектры н-карбоновых кислот, их метиловых и трифторэтиловых эфиров представляют собой две независимых серии ионов: " быструю" неперегруппировочную серию, с превалирующими отрывами C4H8 и "медленную" перегруппировочную серию, с отрывами С2H4.
Высокая интенсивность пиков ионов +CH2CH2C=O(OH) с m/z 73, +CH2CH2C=O(OCH3) с m/z 87 и +CH2CH2C=O(OCH2CF3) с m/z 155, образующихся в неперегруппировочных сериях - результат отрывов С4H8, приводящих к удвоенному отводу избыточной энергии по сравнению с отрывами С2H4, а увеличение числа таких отрывов к большей стабилизации образующихся ионов и росту их интенсивности.
Благодарности
Работа выполнена при поддержке Министерства науки и высшего образования Российской Федерации с использованием научного оборудования Центра исследования строений молекул ИНЭОС РАН.
Список литературы
- Nicholson, A.J.C.,Transaction of the Faraday Society, 1954, 50, 1067.
- McLafferty, Fred W., Anal.Chem., 1959, 31, 82.
- Budzikiewicz H., Djerassi C., Williams D.H. Mass Spectrometry of Organic Compounds. San Francisco, Holden-Day Inc., 1967. 690 p.
- Happ, G.P., Stewart, D.W., J.Am. Chem. Soc. 1952, 74, 4404.
- Вульфсон Н.С., Заикин В.Г., Микая А.И., Масс-спектрометрия органических соединений. М., Химия, 1986, 312 c., стр. 228.
- Тахистов В.В., Практическая масс-спектрометрия органических соединений. Ленинград, 1977, 268 с., стр. 95-96.
- Лебедев А.Т., Масс-спектрометрия в органической химии. Москва, «Бином, Лаборатория знаний», 2003, 493 c., стр. 259-261.
- Каграманов Н.Д., Fluorine notes, 2020, 1(128), 3-4.
- Каграманов Н.Д., Тютюнов А.А. Fluorine notes, 2019, 5(126), 5-6.
- Тахистов В.В. Органическая масс-спектрометрия. Термохимическое описание изомеризации и фрагментации ионов и радикалов в газовой фазе. Ленинград, «Наука», 1990, 221 с, стр.24-25.
Статья рекомендована к публикации членом редколлегии к.х.н. М.А. Манаенковой
Fluorine Notes, 2020, 132, 3-4


