Поступило в редакцию: Май 2019
УДК 542.91; 546.223.3; 547.221; 547.223
Fluorine Notes, 2019, 124, 5-6
Получение 2-бромэтилтетрафторхлорсульфата для синтеза производных бромдифторуксусной кислоты
В.Э. Бойко, В.Л. Дон, С.М. Игумнов
Институт элементоорганических соединений им. А. Н. Несмеянова Российской академии наук, 119991, ГСП-1, Москва, В-334, ул. Вавилова, д. 28
e-mail: boykii@mail.ru
Аннотация: Предложен двухстадийный метод получения этилбромдифторацетата из тетрафторэтилена. Тетрафторэтилен реагирует с хлористым бромом в хлорсульфоновой кислоте с получением 2-бромтетрафторэтилхлорсульфата, который в этаноле под действием основания с хорошим выходом дает этилбромдифторацетат.
Ключевые слова: 2-бромтетрафторэтилхлорсульфат, этилбромдифторацетат, тетрафторэтилен.
Этилбромдифторацетат является важным интермедиатом в синтезе многих фармацевтических препаратов, а также средств защиты растений [1-3], поэтому актуален поиск новых подходов к его получению. Мы предлагаем получение этилбромдифторацетата из 2-бромтетрафторэтилхлорсульфата.
2-Бромтетрафторэтилфторсульфат был получен ранее взаимодействием 1,2-дибромтетрафторэтана с бромфторсульфатом [4], или взаимодействием тетрафторэтилена с бромсукцинимидом и фторсульфоновой кислотой [5]. Бромфторсульфат и фторсульфоновая кислота – высокоагрессивные и труднодоступные реагенты. Нами найдено, что тетрафторэтилен взаимодействует с хлористым бромом в хлорсульфоновой кислоте подобно тому как и с хлористым иодом в хлорсульфоновой кислоте [6] с образованием 2-бромтетрафторэилхлорсульфата, не описанного ранее в литературе. Полученный таким образом 2-бромтетрафторэтилхорсульфат может быть легко превращен в различные производные бромдифторуксусной кислоты. Реакция получения 2-бромтетрафторэтилхорсульфата проводится в открытой системе, без использования реакторов для работы под давлением. Надо отметить, что получение 2-иодтетрафторэтилхлорсульфата также с хорошим выходом проходит в открытой системе, и нет необходимости применения реакторов для работы под давлением, как описано в [6] и в [7].
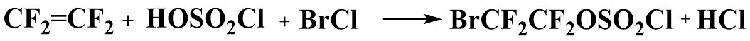
Хлористый бром получают пропусканием газообразного хлора в жидкий бром при охлаждении, при температуре реакционной смеси менее 0°С (хлористый бром устойчив при температурах ниже 5°С). Затем в реакционную смесь добавляют хлорсульфоновую кислоту и, поддерживая температуру в интервале -10°С -0 °С в течение всего процесса, добавляют тетрафторэтилен. Полученный продукт отгоняют из реакционной смеси в вакууме и затем перегоняют при атмосферном давлении. Выход 2-бромтетрафторэтилхорсульфата, представляющего собой жидкость с температурой кипения 112°С, более 90%.
Из 2-бромтетрафторэтилхорсульфата можно получить различные производные бромдифторуксусной кислоты, эфиры, фторангидрид, амид, подобно получению производных иоддифторусксусной кислоты, описанных в [7].
Взаимодействием 2-бромтетрафторэтилхорсульфата (или 2-бромтетрафторэтилфторсульфата) с этиловым спиртом в присутствии основания, такого, как триэтиламин, при охлаждении с хорошим выходом получают этилбромдифторацетат.
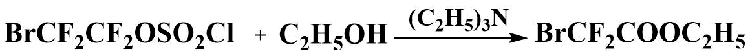
Большинство из известных способов получения этилбромдифторацетата основано на взамодействии галогенангидридов бромдифторуксусной кислоты с этиловым спиртом, сами галогенангидриды получают как правило гидролизом различных 1,1-дифтортетрагалогенэтанов - CF2BrCFClBr, CF2BrCBr2 или CF2BrCF2Br олеумом при катализе соединениями ртути [8-10]. В китайском патенте 2017 года [11] описано окисление 1,1-дифтортетрагалогенэтана озоном с последующим взаимодействием полученной окиси со спиртом с получением этилбромдифторацетата. Известен способ, в котором различные 1,1-дифтортетрагалогенэтаны смешивают со спиртом и каким-либо радикальным инициатором и далее при нагревании окисляют непосредственно газообразным кислородом, разбавленным каким-либо инертом, получая этилбромдифторацетат [12].
Предложенный двухстадийный способ получения бромдифторацетата из тетрафторэтилена удобен для использования в лабораторных условиях, так как не требует никакой специальной аппаратуры, и может быть также масштабирован для промышленного производства.
На способ получения бромдифторацетата получен патент РФ № 2602238.
Экспериментальная часть
ЯМР 1H, 19F спектры записаны на спектрометре “Bruker AVANCE-300” при 300 и 282 MHz соответственно, внешний стандарт CDCl3. Химические сдвиги сигналов 1H спектров определены относительно остаточного сигнала растворителя (CHCl3 δ: 7,26) и даются в м.д. относительно ТМС. Химические сдвиги сигналов в спектрах 19F приведены в м.д. относительно CFCl3. Слабопольные сдвиги имеют положительное значение.
2-Бромтетрафторэтилхлорсульфат
В четырехгорлую круглодонную колбу объемом 2 л, снабженную мешалкой, термометром, барботером, холодильником глубокого охлаждения, заполненным смесью ацетона с сухим льдом, со склянкой Тищенко с конц. H2SO4 на выходе, помещают 230,4 г (1,44 моль) брома и охлаждают на бане ацетон –сухой лед до температуры -10°С. Затем при интенсивном перемешивании барботируют хлор таким образом, чтобы температура реакционной смеси не поднималась выше 0°С. Окончание процесса определяют по привесу реакционной массы (расчетное количество хлора 102,2 г (1,44 моль) , суммарная масса реакционной смеси 332,6 г). Далее реакционную массу перемешивают около 30 минут для завершения реакции.
При температуре 0-(-10)°С при перемешивании и охлаждении в реакционную массу добавляют 685 г (5,9 моль) хлорсульфоновой кислоты и затем барботируют 350 г (3,5 моль) тетрафторэтилена, после чего продукт отгоняют в вакууме из реакционной смеси до температуры кипения 50°С при 50 мм рт.ст. (в кубе остается хлорсульфоновая кислота), и ректифицируют. Получают 940 г 2-бромтетрафторэтилхлорсульфата чистотой 97%. Выход 91%. Температура кипения 112°С.
ЯМР 19F (δ, м.д.): -70,8, (м., 2F, CF2Br), -87,6 (м., 2F, CF2OSO2Cl).
Этилбромдифторацетат
К 15,18 г (0,33 моль) этилового спирта при перемешивании добавляют 0,8 г абсолютного триэтиламина и при охлаждении до 0-5°С и перемешивании добавляют по каплям 32 г (0,11 моль) 2-бромтетрафторэтилхлорсульфата. Далее при той же температуре добавляют еще 4,75 г абсолютного триэтиламина. (Всего добавляют 5,55 г (0,055 моль) триэтиламина). После окончания прибавления реагентов водяную баню убирают и реакционной смеси дают нагреться до комнатной температуры, при этом происходит газовыделение. После чего в реакционную смесь добавляют 70 мл хлористого метилена и воду. Органический слой отделяют, хлористый метилен отгоняют из реакционной смеси, затем продукт отгоняют в вакууме и повторно перегоняют. Получают 15 г (69%) этилбромдифторацетата чистотой 97%.
Т.кип. 111-113°С, ЯМР 1H (δ, м.д.): 1,5 (т.,J=7,0 Гц, 3H, CH3), 4,5 (кв., J=7,0 Гц, 2H, CH2), ЯМР 19F (δ, м.д.): -62,12 (с, CF2Br).
Благодарности
Работа выполнена при поддержке Министерства науки и высшего образования Российской Федерации с использованием научного оборудования Центра исследования строения молекул ИНЭОС РАН.
Список литературы
- Konas, D.W, Coward, J. K., e-EROS Encyclopedia of Reagents for Organic Synthesis, 2005, 1-5.
- Tarui A., Ikebata T., Sato K., Omote M., Ando A., Org.Biomol. Chem., 2014, 12(33), 6484-6489.
- Заявка WO2014004064.
- Фокин А.В., Студнев Ю.Н., Рапкин А.И., Татаринов А.С., Серянов Ю.В., Известия АН СССР, Сер. хим., 1985, №7, 1635-1638.
- Герман Л.С., Савичева Г.И., Известия АН СССР, Сер. хим., 1984, 33(2), 478-479.
- Патент США US5763552, 1998.
- Ming-H. Hung, Lu Long, and Zhen-Yu Yang, JOC, 2004, 69, 198-201.
- Paleta O., Liska F., Posta A., Collect. Czech. Chem. Commun., 1970, 35(4), 1302-1306.
- Dawans, Morel D., Tetrahedron, 1977, 33(12), 1445-1447.
- Европейский патент EP2867228, 2017.
- Патент Китая CN104628559, 2017.
- Патент США US5619023, 1997.
Статья рекомендована к публикации членом редколлегии В.В. Корниловым
Fluorine Notes, 2019, 124, 5-6


