Поступило в редакцию: Февраль 2018
УДК 541.64:547.322:547.422:547.412.92
Fluorine Notes, 2018, 117, 5-6
Cинтез и свойства нового мономера - 1,1'-ди[метакрилоилокси-бис(трифторметил)метил]ферроцена
В.И.Дяченко, О.А.Мельник, Л.Н.Никитин, С.М.Игумнов
Федеральное государственное бюджетное учреждение науки
Институт элементоорганических соединений им. А.Н.Несмеянова РАН, Российская Федерация, 119991, ГСП-1,
Москва, В-334, ул. Вавилова, 28,
e-mail: vic-d.60@mail.ru
Аннотация: Реакцией 1,1'-ди(1-гидрокси-1-трифторметил-2,2,2-трифторэтил)ферроцена и метакрилоилхлорида в присутствии гидрида натрия в безводном диметилформамиде получен 1,1'-ди[метакрилоилокси-бис(трифторметил)метил]ферроцен. Физико-химическими методами установлено его строение, а также способность к радикальной сополимеризации с метилметакрилатом с образованием сшитых сополимеров.
Ключевые слова: 1,1'-ди(1-гидрокси-1-трифторметил-2,2,2-трифторэтил)ферроцен, сополимеризация, 1,1'-ди[метакрилоилокси-бис(трифторметил)метил]ферроцен, гидрофобные покрытия
Фторсодержащие полимеры, в отличие от нефторированных аналогов, обладают высокой гидро- и олеофобностью, устойчивостью к окислению, действию кислот и агрессивных сред. Благодаря этим свойствам все больше возрастает их экспансия в качестве функциональных гидрофобных покрытий в материаловедении, авиа- и автомобилестроении, текстильной промышленности, каждодневном обиходе [1]. В настоящее время, также, интенсивно развиваются исследования в области химии координационных полимеров. Особое место среди них занимают элементоорганические полимеры, имеющие в своем составе ферроценильный заместитель [2, 3]. Ферроценсодержащие полимеры широко востребованы при создании глюкозных биосенсоров [4], для получения органических полиэлектролитов [5], жидкокристаллических полимеров [6], а также композиционных материалов [7]. Ранее мы сообщали о синтезе 1-трифторметил-1-ферроценил-2,2,2-трифторэтилметакрилата [8] и получения на его основе «side-chain» (со)полимеров различного состава [9]. Показано, что незначительная его добавка (3-5%) в качестве сомономера в реакционную массу, при полимеризации метилметакрилата, приводит к существенному повышению температуры термической деструкции образующегося полиметилметакрилата [10].
Целью данной работы является получение нового фторсодержащего мономера (Схема 1), имеющего в циклопентадиенильных кольцах ферроцена две метакрилатные группы, способные вступать в реакцию сополимеризации с виниловыми мономерами, c образованием сшитых полимеров. К тому же, имея в составе своей молекулы ядро ферроцена, экранируемое двумя объемными третичными заместителями, он также способен выступать в качестве антиоксиданта, расширяющего температурные границы применения полимеров с его добавками.
Так, взаимодействием 1,1'-ди(1-гидрокси-1-трифторметил-2,2,2-трифторэтил)ферроцена (1) с избытком хлорангидрида метакриловой кислоты (2) был получен соответствующий 1,1'-ди[метакрилоилокси-бис(трифторметил)метил]ферроцен (3).
Схема 1
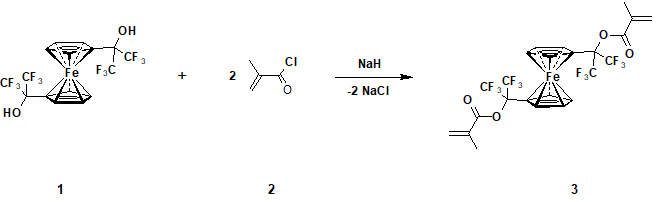
Реакция 1 и 2 легко осуществляется в безводном ДМФА в присутствии гидрида натрия, c образованием 3 с выходом 77% (Схема 1). Исходный для этого синтеза дикарбинол 2 получали реакцией ферроцена и гексафторацетона при катализе трифторуксусной кислотой с выходом 75%, как описано ранее [11]. Следует отметить, что карбинол 2 может быть получен и в отсутствие катализатора при длительном нагревании этих реагентов (180°С, 96 ч) [12]. Сырьем для синтеза целевого содинения 3 являются реагенты, производимые в промышленных масштабах – ферроцен, гексафторацетон и метакрилоилхлорид, что делает его вполне доступным.
Диметакрилат 3 представляет собой кристаллическое красно-оранжевое стабильное при хранении соединение, нерастворимое в воде и растворимое практически во всех органических растворителях. Его строение доказано методом ЯМР 1H и 19F, ИК- и масс-спектроскопии, а также данных элементного анализа. В ИК-спектре 3 присутствуют полосы поглощения, соответствующие фрагментам ферроценильного ядра (полоса валентных СН-колебаний в области 3148 см-1, полоса неплоских деформационных колебаний СН-связей замещенного Сp-кольца в области 854 см-1, полосы в области 1023−1079 см-1, характерные для гомоаннулярных производных ферроцена, и полоса дважды вырожденного антисимметричного валентного колебания Fe-Cp в области 493 см-1). Помимо этого, в спектре соединения 3 присутствуют полосы валентных колебаний С=С при 1634 см-1 и деформационных колебаний С=С при 969, 984 см-1. Также наблюдаются полосы поглощения сложноэфирных связей С=О и С−О в области 1755 и 1135 см-1 соответственно. Имеют место интенсивные полосы при 1224, 1204 см-1, характерные для СF3-групп, и полосы в области 2967 см-1, характерные для СН3-групп.
Благодаря наличию в молекуле двух групп с кратной связью, диметакрилат 3 в присутствии инициатора радикальной полимеризации азоизобутиронитрила при 60-70°С, подобно 1-трифторметил-1-ферроценил-2,2,2-трифторэтилметакрилату [8], способен вступать в реакцию сополимеризации с метилметакрилатом с образованием сшитых полимеров (см. Рис.1).
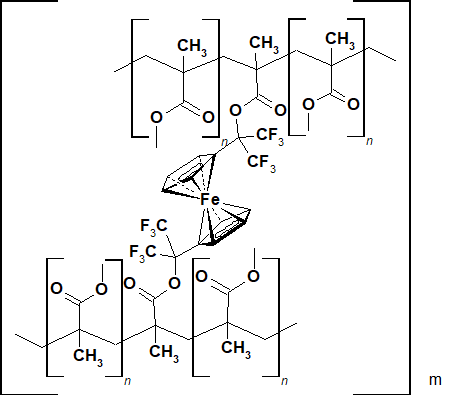
Рис.1
Установлено, что его добавка (1%) в реакционную массу приводит к повышению температуры термической деструкции (Тд), образующегося полиметилметакрилата на 50-55°С на воздухе.
Изучается возможность использования 3 для получения редиспергируемых сополимеров [13,14] с целью повышения контактного угла смачивания θ, образующихся гидрофобных покрытий [15].
Экспериментальная часть
Спектры ЯМР 1Н, 19F зарегистрированы на спектрометре «Bruker Avanse 400» с рабочей частотой 400,13 МГц, 376,5 МГц соответственно. Химсдвиги 1Н приведены относительно ТМС (внутренний стандарт), 19F относительно CF3CO2H - внешний стандарт.
ИК-спектры сняты на спектрофотометре Nicolet Magna-750. Масс-спектры зарегистрированы на квадрупольном масс-спектрометре Finnigan MAT INCOS 50 (прямой ввод, энергия ионизации 70 эВ).
1,1'-Ди[метакрилоилокси-бис(трифторметил)метил]ферроцен (3). К 1,04 г (2 ммоль) карбинола 2 в 5 мл безводного диметилформамида при температуре 20°С и перемешивании порциями прибавляют 0,08 г (2,5 ммоль) 60%-ного гидрида натрия в вазелиновом масле. По окончании выделения водорода к полученному раствору прибавляют 5 мг ионола и затем по каплям 0,29 г (2,5 ммоль) метакрилоилхлорида, поддерживая при этом температуру 20°С. Реакционную смесь перемешивают 2 ч, после чего выливают в 20 мл холодной воды. Продукт реакции экстрагируют петролейным эфиром (2х20 мл), экстракт сушат безводным сульфатом натрия и упаривают в вакууме. Соединение 3 очищают методом колоночной хроматографии на силикагеле, элюент – гексан. Получают 0,9 г красно-оранжевого масла, кристаллизующегося при охлаждении. Выход 77%. Rf=0,55 (СHCI3), т. пл. 4546°С (петролейный эфир).
Спектр ЯМР 1Н, δ, м.д.: 6,19 (уш. с, 1Н,=CН2); 5,73 (уш. с, 1Н,=CН2); 4,49 (уш. с, 8Н, 2С5Н4); 1,95 (уш. с, 6Н, 2СН3). Спектр ЯМР 19F, δ, м.д.: 6,28 (с). Масс-спектр, m/z (Iотн, %): 654 [M]+ (100), 586 (34), 570 (10), 226 (27), 195 (19), 69 (7). Найдено, %: С 44,33; Н 2,71; F 34,78. С24H18F12FeO4. Вычислено, %: C 44,06; Н 2,77; F 34,85. Интенсивный молекулярный ион 654 [M]+(100) соединения 3 свидетельствует о его стабильности, в том числе за счет экранирования СF3-группами, а также способности вступать в редокс-процессы благодаря обратимому изменению валентности железа (Fe2+)/(Fe3+), без изменения геометрии молекулы.
Выводы
Синтезирован новый мономер − 1,1'-ди[метакрилоилокси-бис(трифторметил)метил] ферроцен и изучены его физико-химические свойства. На примере метилметакрилата показана его способность к свободнорадикальной сополимеризации с виниловыми мономерами, приводящая к образованию сшитых сополимеров. Незначительная его добавка (1%) в реакционную массу приводит к повышению температуры термической деструкции Тд, образующегося полиметиметакрилата на 50-55°С на воздухе.
Возможность использования 3 для получения редиспергируемых полимеров с целью повышения контактного угла смачивания θ, образующихся гидрофобных покрытий изучается.
Благодарности
Авторы благодарят Центр структурных исследований ИНЭОС РАН им.А.Н.Несмеянова, Москва за снятие ЯМР 1Н, 19F, ИК- и масс-спектров, а также выполнение элементного анализа.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (проект 16-29-05334-офи-м)
Литература
- Соединения фтора. Синтез и применение, ред. Н. Исикава, перевод с яп., М.: Мир, 1990.
- D. Wohrle, A. Pomogailo. Metal complexes and metals in macromolecules: synthesis, structure and properties. Weinheim: Wiley, 2003, 667 p.
- W.A. Amer, L. Wang, A.M. Amin, L. Ma, H. Yu. J. Inorg. Organomet. Polym. Mater., 2010, 20, 605-615.
- (a) J. Gun, O. Lev, Anal. Chim. Acta., 1996, 336, 95-106; (b) J. Gun, O. Lev, Anal. Lett. 1996, 29, 1933-1938].
- 5. Ye Gao and Jean'ne M. Shreeve, Journal of Polymer Science Part A: Polymer Chemistry, 2005, 43, 5(1), p.974–983.
- S. Senthil, P. Kannan, Journal of Polymer Science Part A: Polymer Chemistry, 2001, 39, 14, p.2396-2403.
- Игумнов С.М., Дяченко В.И., Мельник О.А., Соколов В.И., Никитин Л.Н.// Глава 11 в книге Фторполимерные материалы, ред. В.М. Бузник, Издательство НТЛ, г. Томск, 634050, пл. Новособорная, 1, ISBN 978-5-89503-596-2, 2017,. с.472-503
- В.И. Дяченко, Л.Н. Никитин, О.А. Мельник, С.М. Перегудова, А.С. Перегудов, С.М. Игумнов, А.Р. Хохлов. Fluorine notes, 2011, 79(6).
- О.А. Мельник, В.И. Дяченко, Л.Н. Никитин, И.В. Благодатских, М.И. Бузин, С.М. Перегудова, Я.С. Выгодский, С.М. Игумнов, А.Р. Хохлов. Доклады академии наук, 2012, 443(6), 692-695.
- О.А. Мельник, В.И. Дяченко, Л.Н. Никитин, И.В. Благодатских, М.И. Бузин, Г.Ю. Юрков, Я.С. Выгодский, С.М. Игумнов, В.М. Бузник. Высокомолек. соединения, серия А, 2013, 55 (11), 1315–1320.
- В.И. Дяченко, А.Ф. Коломиец, А.В. Фокин. Тезисы доклада V Всесоюзной конференции по металлоорганической химии, Рига, 1991.
- V. Albrow, A.J. Blake, A. Chapron, C. Wilson, S. Woodwar. Inorg. Chim. Acta, 2006, 359, 1731–1742.
- С.Ю. Тузова, А.Ю. Николаев, Л.Н. Никитин, А.А. Пестрикова, И.Ю. Горбунова, Журнал неорганической химии, 2015, том 60, № 6, с. 800-805.
- С.Ю. Тузова, А.А. Пестрикова, Л.Н. Никитин, А.Ю. Николаев, И.Ю. Горбунова, Е.М. Антипов, Кузьмина М.М., патент РФ 2017 г. № 2610512
- С.Ю. Тузова, А.А. Пестрикова, Л.Н. Никитин, А.Ю. Николаев, патент РФ 2017 г. № 2618253.
Статья рекомендована к публикации членом редколлегии д.х.н. С.Р. Стерлиным
Fluorine Notes, 2018, 117, 5-6


