Поступило в редакцию: Июнь 2017
УДК 10.17677/fn20714807.2017.04.04
Fluorine Notes, 2017, 113, 7-8
Синтез фторсодержащих эфиров 2,5-фурандикарбоновой кислоты
А.М. Сахаров, О.У. Смирнова, А.А. Ярош
Институт органической химии им. Н.Д. Зелинского РАН, 117991, Москва, Ленинский проспект 47.
e-mail: as@zelinsky.ru, yar@ioc.ac.ru
Реферат: Синтезированы фторсодержащие сложные эфиры на основе 2,5- фурандикарбоновой кислоты, а также ее производных и 2,2,3,3,4,4,5,5-Октафторпентанола-1 (спирт-теломер n-2). В качестве катализаторов этерификации применяли серную кислоту, тетрабутоксититан и бисульфат натрия. Контроль за реакцией осуществляли с помощью ЯМР- 1Н, 19F и 13С. Установлено, что при использовании тетрабутоксититана при 125°С происходит его частичная переэтерификация за счет замены бутокси-группы на 2,2,3,3,4,4,5,5-октафторамилокси-группу . Наилучшие результаты получены при проведении реакции с использованием дихлорангидрида 2,5-фурандикарбоновой кислоты.
Ключевые слова: 2,5-фурандикарбоновая кислота, серная кислота, тетрабутоксититан, бисульфат натрия, дихлорангидрид 2,5- фурандикарбоновой кислоты, ЯМР-спектроскопия.
Синтез фторсодержащих сложных эфиров обычно проводят, исходя из ангидридов, хлорангидридов, эфиров фторкарбоновых кислот и фторсодержащих спиртов. Реакцию проводят в условиях кислотного катализа, выход сложных эфиров достигает 73% [1,2]
В качестве алифатической карбоновой кислоты была применена 2,5- фурандикарбоновая кислота (ФДКК), которая является продуктом окисления 5- гидроксиметилфурфураля (5-HMF) - одного из основных синтонов современного органического синтеза. Для синтеза фторсодержащих эфиров предварительно был получен диметиловый эфир (ДМЭФДКК), при кипячении соответствующей кислоты с метанолом в присутствии серной кислоты в качестве катализатора [2]. Выход целевого продукта составил 55%. Строение ДМЭФДКК подтверждено спектрами ЯМР- 1Н и 13С, которые совпадают с литературными данными (схема 1):
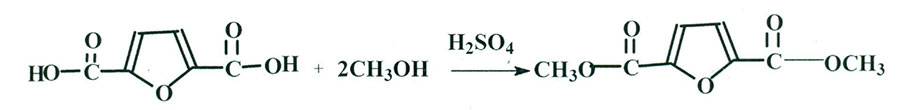
Схема 1
Исследовано несколько путей синтеза целевого соединения - фторсодержащих эфиров 2,5-фурандикарбоновой кислоты (схемы 2-5).
Реакцией переэтерификации ДМЭФДКК при его взаимодействии со спиртом теломером n-2 (схема 2):
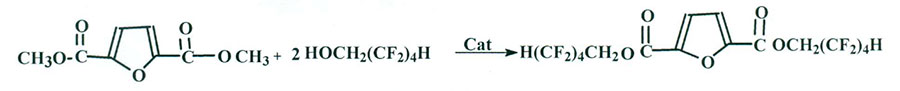
Схема 2
В качестве катализаторов переэтерификации (по схеме 2) использовали H2SO4. СF3СООН, а также Ti(OC4H9)4 (ТБТ) [2-4]. В последнем случае в качестве растворителя использовали ДМФА. Контроль за ходом реакции осуществляли по данным ЯМР 1Н и 19F. В присутствии серной и трифторуксусной кислот продуктов реакции переэтерификации обнаружено не было.
При проведении реакции ДМЭФДКК со спиртом n-2, взятых в мольном соотношении 1:2, и ТБТ в качестве катализатора (мольное соотношение ДМЭФДКК:ТБТ=3:1) в растворе ДМФА было обнаружено образование целевого продукта. Переэтерификацию наиболее удобно было контролировать по спектрам ЯМР 19F, сравнивая интегральные интенсивности сигналов при -127.5 м.д. (группа OCH2CF2 в исходном спирте) и -121 .8 м.д. для группы (COOCH2CF2) в продукте реакции. Кроме того, появлялись сигналы при -127.2 и -132.3 м.д. при сохранении сигналов при -127.5 и -132.3 м.д., характерных для не вступившего в реакцию спирта n-2. Спектры ЯМР 1Н характеризуются наличием сигналов в области 7.23 м.д. (протоны фуранового кольца) и 3.9 м.д. (СН3OOС от ДМЭФДКК) . Сравнение их интегральных интенсивностей совпадало с данными спектра ЯМР 19F.
Было сделано предположение, что ТБТ в данной реакции работает не только в качестве катализатора, но и вступает в реакцию переэтерификацию со спиртом n=2 при 125 °С.
Для выяснения данного обстоятельства была проведена реакция между ТБТ и спиртом при 125 °С в течение 3 часов и мольном соотношении реагентов равном 1:2. В спектре ЯМР- 19F появляются два дублета в областях -127.1- 128.2 и -131.3- 1 132.7 м.д. Сигналы при -122.7 и -139.1 , характерные для сигналов групп CF2CF2, расположенных в середине цепи молекулы спирта n-2, остаются на своих местах.
Из данных спектра ЯМР 13С [м.д.:103-120 [5 триплетов от групп (CF2)4 ; 74.9 (СН2О); 34.0, 17.8 и 12.2 для групп СН2СН2СН3 как в ТБТ] можно заключить, что при 125 °С по крайней мере одна бутокси-группа в ТБТ (Ткип бутанола 117 °С) замещается на алкокси-группу спирта n-2. Таким образом, вывод о том, что ТБТ в исследуемой реакции является не только катализатором, но и реагентом, находит свое экспериментальное подтверждение. При проведении реакции при 150 °С с увеличенным количеством ТБТ (мольное соотношение ДМЭФДКК:ТБТ=1:1) через 10 часов выход целевого продукта достигал 80% (по данным ЯМР-спектроскопии). Однако, с выделением целевого продукта возникли определенные сложности, поэтому был рассмотрен другой метод получения целевого продукта.
Для синтеза фторсодержащих эфиров на основе 2,5-фурандикарбоновой кислоты был применен другой катализатор – NaHSO4 [3], (схема 3).
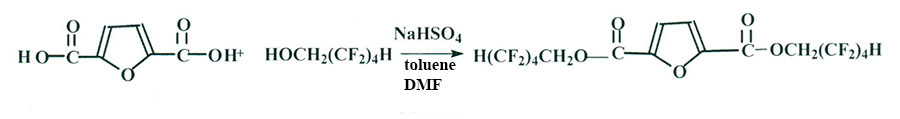
Схема 3
Оказалось, что вследствие очень малой растворимости ФДКК в толуоле реакцию не удается осуществить даже при длительном кипячении свыше 60 часов. Поэтому в реакционную смесь помимо толуола был добавлен ДМФА. Реакцию проводили при 150 °С. При анализе спектров ЯМР- 1 Н, 13C и 19F установлено , что происходит образование фторсодержащего эфира ФДКК, выход которого повышался с увеличением времени реакции и через 60 часов кипячения достигал 70%. В качестве побочного продукта образуется комплексная соль [NаНSО4 х ДМФА]. Выделить целевой продукт в чистом виде не удалось.
Поэтому был предварительно синтезирован дихлорангидрид 2,5-фурандикарбоновой кислоты [5,6] (схема 4) и при его последующем взаимодействии со спиртом n-2 синтезирован с выходом 80% 5Н,2,3,4,5-октафторамил-фуран-2,5 дикарбоксилат - порошкообразный продукт, хорошо растворимый в метаноле, ацетоне, хладоне-113 и гексафторбензоле . Тпл. = 45-47 °С, (схема 5):
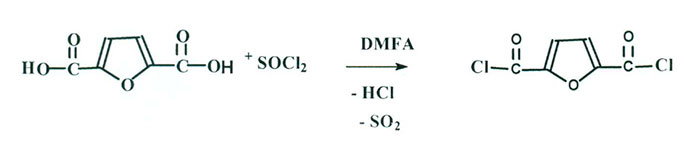
Схема 4
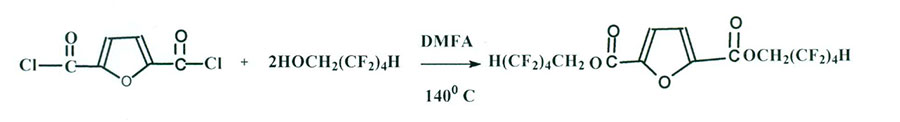
Схема 5
ИК-спектр, ν, см-1 : 3433 (СН фуранового кольца) ; 1748 (С=О сложного эфира); 1134-1114 (CF2).
Спектр ЯМР- 1Н (раствор в C6F6), δ, м.д.: 8.0 (s, 2Н фуранового кольца); 7.29-6.9 (t. CHCF2).
Спектр ЯМР- 19F (раствор в C6F6), δ, м.д.: -139.76 ÷ -140 .0 (d . CF2H); -131 .5 (s. CF2CF2H); -126 .6 (s, CF2CF2CF2H); -121. 1 (s, OCH 2CF2).
Авторы выражают благодарность Российскому научному фонду за финансовую поддержку исследования (грант № 14-50-00126).
Литература
- Robert Filler, Jack V.Fenner, Charles S.Stokers, Josef F. O'Brien and Murray Hauptschein. JACS (19530 75, 2693-2695. Fluorinated Esters. 111 . Diesters of Carboxylic Acids with Fluorine-containing Alcohols and Glycols. DOI: 10.1021/ja01107а042.
- Bernardm М., Woolf С. US 3438946 а 19690415. Fluoroalkyl-substitution esters, diesters, and polymers therefrom.
- Shanmugam Thiyagarajan, Aliaksei Puki n, Jacco van Haveгen, Martin Lutz, Dаап S. vаn Es. RSC Adv. 2013, 3 ,15678-15686. Concurrent formation of furan-2,5- and furan-2,4-dicardoxylic acid: unexpected aspects of the Henkel reaction .
- Кичура Д.Б., Югач О.В. Химическая промышленность, 7, 1975, 19-21. Этерификация фталевого ангидрида спиртами, используя титансодержащие катализаторы.
- Zhang, Rong; Song Huaijun; Wu, Guowang ; Jiang, Liping; Zeng, Xiaouan ; Huang, Zhuowang; Ding, Jianzhong . Faming Zhuanli Shenqing (2013), CN l 03469348 А 20131225. Fluorinated polybutylene terephthalate drawn textured уаrn fiber and its preparation method.
- С. Morales-Huerta, Juan; М. De Harduya, Antxon; Polymer (UK) 2016, vol. 87, р. 148-158.
Статья рекомендована к публикации членом редколлегии д.х.н. С.М. Игумновым
Fluorine Notes, 2017, 113, 7-8


