Поступило в редакцию: Июль 2017
УДК 10.17677/fn20714807.2017.04.02
Fluorine Notes, 2017, 113, 3-4
Фторирование некоторых функционализированных циклоалкенов путем эпоксидирования и раскрытия оксирана с помощью Deoxofluor* или XtalFluor-E*
Attila Márió Remete,1 Ferenc Fülöp,1,2 Loránd Kiss1*
1Institute of Pharmaceutical Chemistry, University of Szeged, H-6720 Szeged, Eötvös u. 6, Hungary
2MTA-SZTE Stereochemistry Research Group, Hungarian Academy of Sciences, H-6720 Szeged, Eötvös u. 6, Hungary
Email: kiss.lorand00@gmail.com
Графическая аннотация:

Аннотация: Описан удобный, простой синтетический метод для получения некоторых фторсодержащих высокофункциональных производных циклоалканов. Метод синтеза включает в себя стереоселективное эпоксидирование отобранных замещенных циклогексенов с последующим региоселективным раскрытием эпоксидов с помощью Deoxofluor (bis(2-methoxyethyl)aminosulfur trifluoride, CH3OCH2CH2)2NSF3). and XtalFluor-E (Diethylamino)difluorosulfonium tetrafluoroborate) при различных условиях.
Ключевые слова: Циклоалканы,оксиран, фторирование, селективность.
Введение
Эпоксидирование двойной связи углерод-углерод и раскрытие кольца получающихся оксиранов при взаимодействии с множеством нуклеофилов является широко распространенным методом введения различных функциональных групп в скелет органического остова [1-5].
Ввиду большой важности фторированных биомолекул для разработки лекарств, введение одного или более атомов фтора в органическую молекулу на протяжении последних десяти лет вызывает большой интерес [6-10]. Принимая во внимание значимость атома фтора в органической молекуле, раскрытие эпоксида при помощи фторида, несомненно, очень эффективный подход для введения атома фтора в конкретную молекулу [11-13]. Многочисленные синтетические подходы, включая асимметрический, были разработаны для раскрытия эпоксида при помощи фторида. Некоторыми из таких являются фторсодержащие вещества, такие как пиридин·HF [14-15], Et3N·3HF [16], BF3·OEt2 [17], HBF4 [18], KHF2 [19], TBAF/KHF2, TBAF·3H2O/KF [20], KHF2/18-краун-6/хиральный хромовый комлекс Якобсена [21], AgHF2 с рутениевым катализатором [22], а также бензоил фторид с основанием и гексафторизопропанолом [23]. Несмотря на такое изобилие реагентов, стереоселективные и региоселективные трансформации различных функционализированных алициклических фрагментов по-прежнему представляют сложность. Бициклические оксиран-соединенные кольцевые системы, в частности, до сих пор считаются сложными субстратами для раскрытия кольца при помощи фторида. Таким образом, однозначно имеется необходимость для развития новых методов с учетом данного способа фторирования.
Результаты и обсуждение
Целью данной статьи является описание метода синтеза, основанного на окислительном превращении замещенных циклогексенов путем эпоксидирования с последующим нуклеофильным раскрытием трехчленной O-гетероциклической кольцевой системы при помощи фторида с использованием Deoxofluor или XtalFluor-E. Это продолжение нашего исследования химического поведения различных эпокси-2-аминоциклогексан- или циклопентанкарбоксилатов в селективных фторированиях, описанных в недавней статье [24]. Помимо изучения участия соседних функциональных групп, также было исследовано синергетическое влияние одновременного присутствия карбоксилата и N-защищенных амино фрагментов на результаты фторирования. Таким образом, принимая во внимание ранее полученные результаты, мы описываем раскрытие нкоторых оксиранов, содержащих только одну функциональную группу на циклогексеновом скелете: или карбоксилат, или защищенную амино-группу.
Наше экспериментальное исследование началось с коммерчески доступного рацемического этилциклогексен-3-карбоксилата (±)-1, который был подвергнут эпоксидированию, согласно описанной в литературе методике [25]. В связи со стериохимическими факторами, эфиры эпоксициклогексена (±)-2 и (±)-4 имеют выходы 55% и 29%, соответственно. Попытки раскрытия эпоксидного кольца в (±)-2 предпринимались при различных условиях в зависимости от фторирующего реагента (Deoxofluor или XtalFluor-E), растворителя (CH2Cl2, THF или 1,4-dioxane) и температуры. К сожалению, Deoxofluor не позволил получить какой либо идентифицируемый продукт. После нескольких попыток мы обнаружили, что раскрытие оксиранового кольца происходит при наличии 2 эквивалентов XtalFluor-E, в присутствии Et3N HF в кипящем диоксане, с региоселективностью приводящей через фторидную атаку на С-6 к фторсодержащему продуктуt. Структура продукта фторгидрина (±)-3 была определена на основе данных 2D ЯМР (Схема 1). Необходимо отметить, что ни использование большего количества реагента XtalFluor-E, ни Deoxofluor не обеспечили получение ожидаемого гидрокси-фтор продуктов замещения, а были получены только либо непрореагировавший исходный эфир, либо материалы разложения.
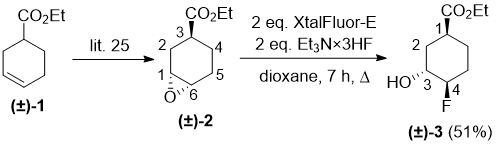
Схема 1
Региоселективность вышеуказанной реакции можно объяснить хорошими диаксиальными конформациями во время раскрытия оксирана. Атака фторид-иона на оксирановое кольцо на позиции C-6 приводит к тому, что предпочтительная поддержка диаксиальной конформации с гидроксилом и фтором в исходных положениях приводит 4-фторированному производному. Атака фторид иона на оксирановое кольцо в позиции C-1 генерирует нежелательные искажения диаксиальной конформации кресла со фтором и гидроксид группами на диаксиальных направлениях; таким образом, соответствующее 3-фторпроизводное получено не было (Схема 2; Следует отметить различие в нумерации эпоксидной системы и фторзамещенного продукта!).
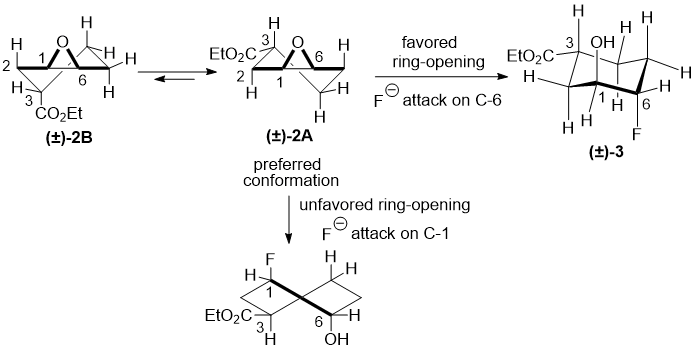
Схема 2.
Следующий эпоксид (±)-4 подвергался фторированию при различных условиях. 2 эквивалента XtalFluor-E индуцировали раскрытие оксиранового кольца в присутствии Et3N·HF в кипящем диоксане и региоселективно дали фторированный продукт, который был идентифицирован согласно 2D ЯМР как соединение (±)-5, с атомом фтора, присоединенным к C-3 циклогексанового скелета.
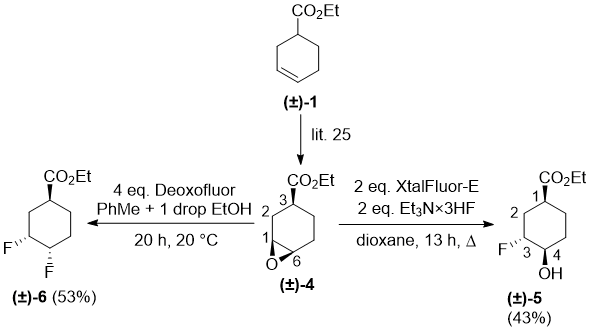
Схема 3.
Опять же, региоселективность раскрытия данного эпоксида можно объяснить хорошей диаксиальной конфирмацией кресла как показано на схеме 4.
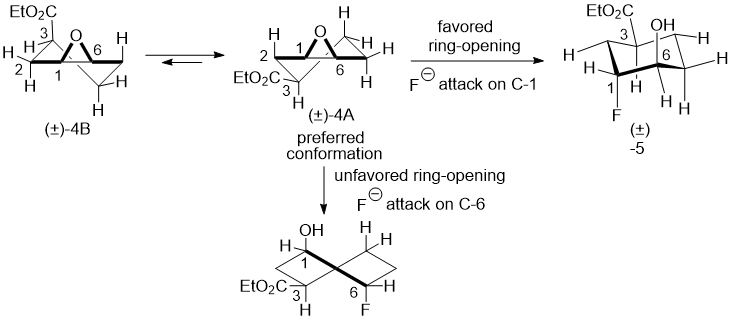
Схема 4.
Последующие попытки заменить вновь созданную гидрокси группу в (±)-5 на фтор, как с помощью XtalFluor-E так и с помощью Deoxofluor не принесло результатов. Примечательно то, что вопреки поведению эпоксида (±)-2, стереоизомер (±)-4 с 4 эквивалентами Deoxofluor и одной каплей EtOH в толуоле превратился во фторированный продукт, идентифицированный как (±)-5. Данное вещество было получено в региоселективном раскрытии оксирана и гидрокси-фтор замещении через конфигурационную иныерсию (Схема 3).
Далее были проведены исследования на амино-земещенном циклогексене. Cbz (Carboxybenzyl)-защищенный циклогексен (±)-8, полученный из имеющегося в продаже циклогекс-3-ен карбоновой кислоты (±)-7 [26], был подвержен эпоксидированию с м-метахлорпероксибензойной кислотой, давая только один стереоизомер, идентифицированный как (±)-9 в cis-диасетереоселективном виде. В этом продукте, карбаматная группа и оксирановое кольцо имеют одинаковое пространственное расположение относительно шестичленного кольца. Стереоселективность данной реакции может быть приписана влиянию присоединенных атомов водорода в процессе промежуточного состояния окисления [27, 28]. Как ни удивительно , фторирование (±)-9 с XtalFluor-E не дало какой либо идентифицируемый продукт. В противоположность, реакция с Deoxofluor, индуцированная фторированием, через региоселективное раскрытие эпоксида, с последующим гидрокси-фтор взаимным преобразованием приводит к получению двуфтористого производного (±)-10 в качестве единственного продукта (Схема 5). Сравнение этого с аналогичным процессом для получения (±)-6 показано на Схеме 3.
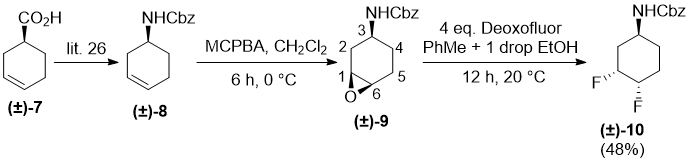
Схема 5.
Выводы
Для получения высокофункционализированных фторсодержащих аллильных структур были изучены циклогексильные производные в качестве модельных субстратов в процессе окисления с последующим фторированием. Метод синтеза основан на эпоксидировании кольцевой ненасыщенной связи с последующим раскрытием кольца образующегося функционализированного замкнутого циклогексильного оксирана с помощью XtalFluor-E и Deoxofluor, используемых в качестве фторирующих реагентов.
Экспериментальная часть
Общая информация:
Химические реактивы были закуплены в Sigma-Aldrich. Используемые растворители были получены от поставщиков. Температура плавления определялась на приборе Кофлера. Элементные анализы были получены на приборе Perkin–Elmer CHNS-2400 Ser II. Силикагель 60 F254 был закуплен в Merck. Спектры ЯМР записывались при комнатной температуре на приборе Bruker Avance 400 spectrometer with 11.75 T magnetic field strength (1H частота 400.13 МГц; 19F частота 376.50 МГц, 13C частота 100.76 МГц) в CDCl3 или D6-DMSO растворе, используя дейтериевый сигнал растворителя, чтобы ограничить поле. 1H и 13C химические сдвиги даны относительно TMS и 19F относительно CFCl3 (0.00 ppm).
Ethyl (1S*,3R*,6R*)-7-oxabicyclo[4.1.0]heptane-3-carboxylate and ethyl (1R*,3R*,6S*)-7-oxabicyclo[4.1.0]heptane-3-carboxylate
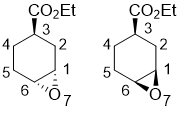
В раствор этил циклогекс-3-енкарбоксилата (1.87 г, 12.1 ммоль) в CH2Cl2 (75 mL) добавляли 3-хлорпербензойной кислоты (1.2 эквивалента). После перемешивали в течение 2 часов при комнатной температуре, затем реакционную смесь разбавляли CH2Cl2 (70 мл), промывали раствором Na2SO3 (1.3 г в 30 мл насыщенного раствора NaHCO3 растворе), затем промывали с 2 × 30 мл насыщенного раствора NaHCO3. Органический слой сушили (Na2SO4) и концентрировали. Смесь продукта отделяли путем колоночной хроматографии на силикагеле (n-hexane/EtOAc). Выходы: 55% этил (1S*,3R*,6R*)-7-oxabicyclo[4.1.0]heptane-3-carboxylate и 29% этил (1R*,3R*,6S*)-7-oxabicyclo[4.1.0]heptane-3-carboxylate (lit. 25).
Benzyl (1S*,3S*,6R*)-7-oxabicyclo[4.1.0]heptan-3-ylcarbamate
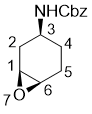
Бензил циклогекс-3-ен-1-илкарбамата (0.50 г, 2.16 ммоль) растворяли в CH2Cl2 (25 мл), охлаждали до 0 °C, затем добавляли 3-хлорпербензойную кислоту (1.2 эквивалента). После перемешивания в течении 4 часов, в течении которых позволили реакционной смеси нагреться до комнатной температуры, реакционную смесь разбавляли CH2Cl2 (25 мл), промывали раствором Na2SO3 (0.5 г в 25 мл насыщенного раствора NaHCO3), затем мыли 2 × 25 мл насыщенного ратвора NaHCO3. Органический слой сушили (Na2SO4) и концентрировали. Сырой продукт очищали путем колоночной хроматографии на силикагеле (n-hexane/EtOAc).
Белое твердое вещество; Выход: 75%; Rf = 0.50 (n-hexane/EtOAc 3:2); Mp 56-65 °C. 1H-NMR (400 MHz, D6-DMSO, TMS) δ = 1.18-1.31 (m, 1H, H-4), 1.34-1.43 (m, 1H, H-4), 1.52-1.62 (m, 1H, H-2), 1.75-1.87 (m, 1H, H-5), 1.98-2.07 (m, 1H, H-5), 2.12-2.22 (m, 1H, H‑2), 3.01-3.09 (m, 2H, H-1 and H-6), 3.21-3.28 (m, 1H, H-3), 4.99 (s, 2H, OCH2), 7.08 (d, J = 7.40 Hz, 1H, NH), 7.27-7.40 (m, 5H, CH-Ar). 13C NMR (100 MHz, D6-DMSO, TMS) δ = 24.6, 25.5, 31.0, 46.2, 51.2, 51.8, 66.0, 128.6, 129.2, 138.1, 156.1. MS (ESI, pos) m/z 248 (M + 1). Anal. Calcd. for C14H17NO3: C, 68.00; H, 6.93; N, 5.66. Found: C, 67.69; H, 6.66; N, 5.31.
Раскрытие оксиранового кольца с помощью фторида:
Способ A
В раствор исходного эпоксида (0.50–0.75 ммоль) в безводном толуоле (10 мл) в атмосфере аргона добавляли одну каплю EtOH и 50% Deoxofluor в толуоле (4 эквивалента) затем раствор перемешивали при температуре 20 °C в течение времени, указанного в статье. Затем раствор разбавляли CH2Cl2 (30 мл) и органический слой отмывали насыщенным раствором NaHCO3 (2 × 20 мл). Органический слой сушили (Na2SO4) и концентрировали. Сырой продукт очищали путем колоночной хроматографии на силикагеле (n-hexane/EtOAc).
Способ B
В раствор исходного эпокида (0.50–0.75 ммоль) в 1,4-диоксане (10 мл) в атмосфере аргона добавляли Et3N·3HF (2 эквивалента), затем добавляли XtalFluor-E (1 эквивалент). Реакционная смесь кипятили в течение времени, указанного в статье. Раствор после охлаждения разбавляли CH2Cl2 (30 мл) и органический слой мыли насыщенным раствором NaHCO3 (2 × 20 мл). Органический слой сушили (Na2SO4) и концентрировали. Сырой продукт очищали путем колоночной хроматографии на силикагеле (n-hexane/EtOAc or n‑hexane/acetone).
Ethyl (1S*,3R*,4R*)-4-fluoro-3-hydroxycyclohexanecarboxylate
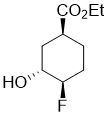
Бесцветное масло; Выход 51%; Rf = 0.47 (n-hexane/EtOAc 2:1). 1H-NMR (400 MHz, CDCl3, TMS) δ = 1.27 (t, J = 7.12 Hz, 3H, CH3), 1.56-1.83 (m, 3H, H-2, H-5 and H-6), 1.89-2.09 (m, 2H, H-5 and H-6), 2.19-2.31 (m, 1H, H-2), 2.67-2.79 (m, 1H, H‑1), 3.90-4.02 (m, 1H, H-3), 4.16 (q, J = 7.12 Hz, 2H, OCH2), 4.28-4.49 (m, 1H, H-4). 19F NMR (376 MHz, CDCl3) δ = -184.71. 13C NMR (100 MHz, CDCl3, TMS) δ = 14.6, 24.3 and 24.4 (3J = 7.21 Hz), 26.7 and 26.9 (2J = 19.17 Hz), 32.2 and 32.3 (3J = 3.64 Hz), 38.1, 61.0, 69.1 and 69.3 (2J = 22.58 Hz), 92.9 and 94.6 (1J = 172.97 Hz), 174.9. Anal. Calcd. for C9H15FO3: C, 56.83; H, 7.95. Found: C, 56.53; H, 7.69.
Ethyl (1S*,3R*,4R*)-3-fluoro-4-hydroxycyclohexanecarboxylate
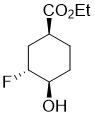
Бесцветное масло; Выход 43%; Rf = 0.41 (n-hexane/acetone 4:1). 1H-NMR (400 MHz, CDCl3, TMS) δ = 1.27 (t, J = 7.12 Hz, 3H, CH3), 1.51-1.69 (m, 2H, H-5 and H-6), 1.74-1.86 (m, 1H, H-2), 1.86-2.07 (m, 2H, H-5 and H-6), 2.23-2.41 (m, 1H, H-2), 2.70-2.79 (m, 1H, H-1), 3.73-3.84 (m, 1H, H-4), 4.15 (q, J = 7.12 Hz, 2H, OCH2), 4.49-4.70 (m, 1H, H-3). 19F NMR (376 MHz, CDCl3) δ = -185.90. 13C NMR (100 MHz, CDCl3, TMS) δ = 14.6, 24.3, 28.4 and 28.5 (3J = 3.76 Hz), 30.2 and 30.4 (2J = 19.83 Hz), 38. 8 and 38.9 (3J = 7.28 Hz), 61.1, 70.5 and 70.7 (2J = 22.29 Hz), 91.8 and 93.5 (1J = 171.89 Hz), 174.7. Anal. Calcd. for C9H15FO3: C, 56.83; H, 7.95. Found: C, 56.51; H, 8.38.
Ethyl (1S*,3R*,4S*)-3,4-difluorocyclohexanecarboxylate
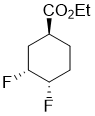
Бесцветное масло; Выход 53%; Rf = 0.47 (n-hexane/EtOAc 9:1). 1H-NMR (400 MHz, CDCl3, TMS) δ = 1.26 (t, J = 7.14 Hz, 3H, CH3), 1.49-1.64 (m, 1H, H-6), 1.70-1.88 (m, 1H, H-2), 1.88-2.14 (m, 3H, 2 × H-5 and H-6), 2.26-2.39 (m, 1H, H-2), 2.66-2.76 (m, 1H, H-1), 4.14 (q, J = 7.12 Hz, 2H, OCH2), 4.41-4.67 (m, 1H, H-4), 4.84-5.06 (m, 1H, H‑3). 19F NMR (376 MHz, CDCl3) δ = -188.58, -200.35. 13C NMR (100 MHz, CDCl3, TMS) δ = 14.6, 25.4 and 25.5 (3J = 9.91 Hz), 25.7 and 25.7 and 25.9 and 25.9 (2J = 19.96 Hz, 3J = 3.33 Hz), 31.2 and 31.2 and 31.4 and 31.4 (2J = 20.34 Hz, 3J = 5.59 Hz), 37.1 and 37.2 (3J = 2.93 Hz), 61.1, 87.4 and 87.6 and 89.2 and 89.3 (1J = 177.81 Hz, 2J = 17.43 Hz), 89.3 and 89.5 and 91.1 and 91.3 (1J = 181.41 Hz, 2J = 18.18 Hz), 174.8. Anal. Calcd. for C9H14F2O2: C, 56.24; H, 7.34. Found: C, 55.88; H, 6.99.
Benzyl (1S*,3R*,4S*)-3,4-difluorocyclohexyl)carbamate
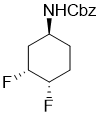
Белый твердый; Yield 48%; Rf = 0.53 (n-hexane/EtOAc 2:1); Mp 102-106 °C. 1H-NMR (400 MHz, D6-DMSO, TMS) δ = 1.27-1.43 (m, 1H, H-6), 1.50-1.71 (m, 1H, H-2), 1.72-1.95 (m, 3H, H-6 and 2 × H-5), 2.01-2.17 (m, 1H, H-2), 3.56-3.72 (m, 1H, H-1), 4.57-4.84 (m, 1H, H-4), 4.85-5.12 (m, 3H, H-3 and OCH2), 7.21-7.44 (m, 6H, CH-Ar and NH). 19F NMR (376 MHz, D6-DMSO) δ = -185.60, -196.57. 13C NMR (100 MHz, D6-DMSO, TMS) δ = 25.3 and 25.5 (2J = 20.04 Hz), 28.6, 34.6 and 34.8 (2J = 19.21 Hz), 45.2, 66.2, 88.7 and 88.9 and 90.4 and 90.6 (1J = 174.10 Hz, 2J = 17.29 Hz), 89.5 and 89.7 and 91.3 and 91.4 (1J = 178.17 Hz, 2J = 17.80 Hz), 128.7, 129.2, 138.0, 156.3. MS (ESI, pos) m/z 270 (M + 1). Anal. Calcd. for C14H17F2NO2: C, 62.44; H, 6.36; N, 5.20. Found: C, 62.10; H, 6.09; N, 4.86.
Благодарности
Мы благодарим Hungarian Research Foundation (NKFIH Nos. K 115731 and K 119282) за финансовую поддержку. Мы также благодарим за поддержку по гранту GINOP-2.3.2-15-2016-00014. Данное исследование также поддержано EU-funded Hungarian grant EFOP-3.6.1-16-2016-00008.
Литература
- Wang, P. A. Beilstein J. Org. Chem. 2013, 9, 1677-1695.
- Zhu, Y.; Wang, Q.; Cornwall, R. G.; Shi, Y. Chem. Rev. 2014, 114, 8199-8256.
- Chawla, R.; Singh, A. K.; Yadav, L. D. S. RSC Adv. 2013, 3, 11385-11403.
- Meninno, S.; Lattanzi, A. Chem. Eur. J. 2016, 22, 3632- 3642.
- Kiss, L.; Remete, A. M.; Nonn, M.; Fustero, S.; Sillanpaa, R.; Fülöp, F. Tetrahedron 2016, 72, 781-787 (and references cited therein).
- Zhou, Y.; Wang, Y.; Gu, Z.; Wang, S.; Zhu, W.; Acena, J. L.; Soloshonok, V. A.; Izawa, K.; Liu, H. Chem. Rev. 2016, 116, 442-518.
- Wang, J.; Sánchez-Roselló, M.; Aceña, J. L.; del Pozo, C.; Sorochinsky, A. E.; Fustero, S.; Soloshonok, V. A.; Liu, H. Chem. Rev. 2014, 114, 2432-2506.
- O’Hagan D. J. Fluorine Chem. 2010, 131, 1071-1081.
- Kiss, L.; Forró, E.; Fustero, S.; Fülöp, F. Eur. J. Org. Chem. 2011, 4993-5001.
- Nonn, M.; Kiss, L.; Haukka, M.; Fustero, S.; Fülöp, F. A Org. Lett. 2015, 17, 1074-1077 (and references therein).
- Champagne, P. A.; Desroches, J.; Hamel, J. D.; Vandamme, M.; Paquin, J. F. Chem. Rev. 2015, 115, 9073-9174.
- Wu, J. Tetrahedron Lett. 2014, 55, 4289-4294.
- Liang, T.; Neumann, C. N.; Ritter, T. Angew. Chem. Int. Ed. 2013, 52, 8214-8264.
- Husstedt, W. S.; Wiehle, S.; Stillig, C.; Bergander, C.; Grimme, S.; Haufe, G. Eur. J. Org. Chem. 2011, 355-363.
- O’Hagan, D. J. Org. Chem. 2012, 77, 3689-3699.
- Bykova, T.; Al-Maharik, N.; Slawin, A. M. Z.; O’Hagan, D. Org. Biomol. Chem. 2016, 14, 1117-1123.
- Fraile, J. M.; Mayoral, J. A.; Salvatella, L. J. Org. Chem. 2014, 79, 5993-5999.
- Cresswell, A. J.; Davies, S. G.; Lee, J. A.; Morris, M. J.; Roberts, P. M.; Thomson, J. E. J. Org. Chem. 2012, 77, 7262-7281.
- Kondapi, V. P. K.; Soueidan, O. M.; Hosseini, S. N.; Jabari, N.; West, F. G. Eur. J. Org. Chem. 2016, 1367-1379.
- Yan, N.; Fang, Z.; Liu, Q. Q.; Guo, X. H.; Hu, X. G. Org. Biomol. Chem. 2016, 14, 3469-3475.
- Haufe, G.; Bruns, S.; Runge, M. J. Fluorine Chem. 2001, 112, 55-61.
- Althaus, M.; Togni, A.; Mezzetti, A. J. Fluorine Chem. 2009, 130, 702-707.
- Kalow, J. A.; Doyle, A. G. J. Am. Chem. Soc. 2011, 133, 16001-16012.
- Remete, A. M.; Nonn, M.; Fustero, S.; Fülöp, F.; Kiss, L. Molecules 2016, 21, 1943.
- Goss, R. J. M.; Lanceron, S.; Roy, A. D.; Sprague, S.; Nur-e-Alam, M.; Hughes, D. L.; Wilkinson, B.; Moss, S. J. ChemBioChem 2010, 11, 598-702.
- Ábrahámi, R. A.; Kiss, L.; Fustero, S.; Fülöp, F. Synthesis 2017, 49, 1206–1213.
- Kiss, L.; Remete, A. M.; Nonn, M.; Fustero, S.; Sillanpaa, R.; Fülöp, F. Tetrahedron 2016, 72, 781-787.
- Kiss, L.; Forró, E.; Sillanpää, R.; Fülöp, F. J. Org. Chem. 2007, 72, 8786-8790.
Данные 1H-NMR и 13C-NMR спетров см. английскую версию статьи.
Статья рекомендована к публикации членом редколлегии проф. József Rábai
Fluorine Notes, 2017, 113, 3-4


