Поступило в редакцию: Июль 2017
УДК 547.057, 547.7/.8, 547.1'1.
Fluorine Notes, 2017, 113, 1-2
Синтез (индолил-3)перфторалкилкарбинолов путем взаимодействия индолов с перфторированными альдегидами
Д.В. Гусев, Е.В. Беляева , А.Л. Сиган , Н.Д. Чкаников
ФГБУ ИНЭОС им. А. Н. Несмеянова РАН, 119991, ГСП-1, Москва, В-334, ул. Вавилова, д. 28
e-mail: faftor.belyaeva@mail.ru
Аннотация: Показано что (индолил-3)перфторалкилкарбинолы могут быть получены путем некаталитического селективного гидроксиалкилирования индолов перфторалифатическими альдегидами c различной длиной углеродной цепи или их полуацеталями.
Ключевые слова: перфторалифатические альдегиды, гидроксиалкилирование, индолы, индолил-3-карбинолы
(Индолил-3)перфторалкилкарбинолы с различной конфигурацией перфторалифатической части (RF) имеют практическое значение в качестве предшественников для получения различных биологически активных соединений [1-4].
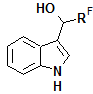
В литературе описано получение индолил-3-карбинолов с RF = CF3, гораздо меньше примеров с RF = C2F5. Среди известных методов синтеза таких соединений следует выделить восстановление 3-ацилиндолов [5-7], присоединение реактива Руперта к индолил-3-карбальдегиду и его производным [8, 9], присоединение перфторалифатических альдегидов и их производных к индолу под действием различных катализаторов с возможностью получения оптически чистых индолил-3-карбинолов [10-12], а также гидроксиалкилирование индолов полифторалифатическими спиртами в присутствии радикальных инициаторов [13]. В нескольких работах упоминается некаталитическое взаимодействие трифторацетальдегида с индолом при комнатной температуре [14] и при нагревании [15]. Примеров реакции длинноцепочечных перфторалифатических альдегидов с индолами в литературе не найдено, поэтому изучение таких реакций расширяет возможности синтетического использования перфторалифатических карбонильных соединений.
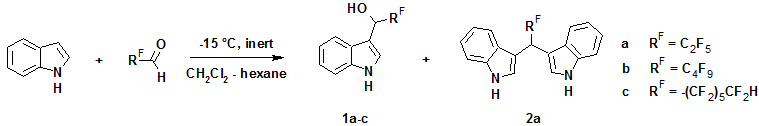
В данной работе показано, что при взаимодействии индола или N-метилиндола с перфторалифатическими альдегидами в инертной атмосфере и без использования катализаторов наблюдается образование соответствующих индолил-3-карбинолов (1а-с и 3а-с) с выходами 41-69%. Как известно, перфторалифатические альдегиды, особенно с короткой перфторуглеродной цепью, являются летучими, гигроскопичными и светочувствительными соединениями, поэтому реакции с ними проводились без доступа света, в инертной атмосфере и при пониженной температуре. Кроме того, тщательный подбор растворителя позволил максимально упростить процесс выделения продуктов реакции. Так, при использовании смесей хлористый метилен – гексан в различных сочетаниях ( от 1:1 до 3:1) 3-замещенные продукты в большинстве случаев выпадали в осадок из реакционной смеси и не требовали дополнительной очистки.
Следует отметить, что в случае реакции перфторпропаналя с незамещенным индолом кроме основного индолил-3-карбинола 1a в качестве побочного образуется соединение 2а - продукт конденсации 1a со второй молекулой индола. В синтезе соединений 1b,c образования побочных продуктов такого типа не наблюдалось. Такое отличие от 1a может быть связано с тем, что 1b,c выпадают в осадок из реакционной смеси, а 1a остается в растворе и повышается вероятность его взаимодействия со второй молекулой индола.
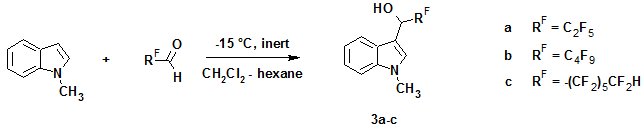
Взаимодействие N-метилиндола с соответствующими альдегидами приводило к образованию только индолил-3-карбинолов (3a-c) с хорошими выходами (53-65%), которые существенно снижались при проведении реакций на воздухе.
Как уже отмечалось использование перфторалифатических альдегидов, особенно с короткой перфторуглеродной цепью, требует специальных условий хранения и проведения реакции. В связи с этим была исследована возможность использования в рассматриваемых реакциях в тех же условиях более стабильной метил полуацетали перфторпропаналя. Оказалось, что при низкой температуре (-15оС, хлористый метилен-гексан=3:1, 3 дня) реакция с образованием 1а (по данным ТСХ) протекает очень медленно, но без образования побочных продуктов.
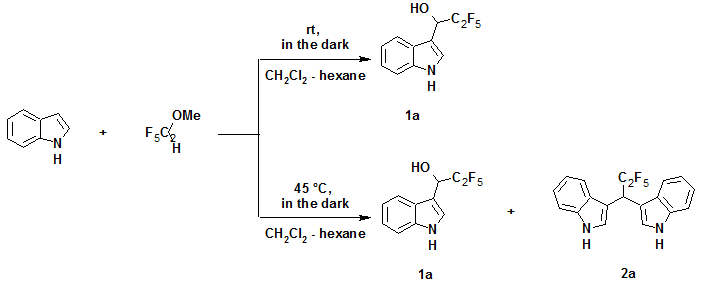
С увеличением температуры до комнатной скорость реакции возрастала, выход продукта 1а за то же время увеличивался до 15%, оставалось заметное количество непрореагировавшего индола, образования побочного продукта 2a (по ТСХ) не наблюдалось. Это может быть связано с присутствием метанола, образующимся в процессе реакции. Наконец полная конверсия индола достигалась при нагревании смеси индола с метил полуацеталью в соотношении 1:2 до 45°С в запаянной ампуле, закрытой от света, в течение 30-ти часов с образованием смеси продуктов 1a и 2a в соотношении 2:3 (общий выход ~70%). По-видимому, значительное увеличение доли продукта 2a в данном случае обусловлено повышением температуры реакции, что увеличивает вероятность конденсации 1a со второй молекулой индола.
Таким образом, в данной работе показана принципиальная возможность некаталитического селективного гидроксиалкилирования индолов с использованием перфторальдегидов в мягких условиях, а полученные (индолил-3)перфторалкилкарбинолы могут найти применение в синтезе биологически активных соединений.
Экспериментальная часть
Спектры ЯМР 1H и 19F регистрировали на спектрометрах Bruker AMX-400 и AMX-300 с частотой 400.13 и 376.50 MГц при 20 0С, отнесение сигналов проведено относительно сигнала остаточных протонов растворителя (dmso-d6) и трифторуксусной кислоты (TFA) в качестве внешнего стандарта.
Масс-спектры (EI-DIP) регистрировали на масс-спектрометре Finnigan Polaris Q, энергия ионизирующего излучения 70эВ, способ ввода образца - прямой ввод.
Ход реакций контролировали методом ТСХ на пластинках Merck Kieselgel 60 F254. Для колоночной хроматографии использовали силикагель MN Kieselgel 60.
Реактивы и растворители: Хлористый метилен (ДХМ) сушили над CaH2 и перегоняли. Индол очищали перекристаллизацией из гексана, N-метилиндол перед использованием перегоняли. Фторсодержащие альдегиды перегоняли над конц. H2SO4 непосредственно перед использованием. Гидраты перфторированных альдегидов и полуацеталь перфторпропаналя использовались производства фирмы “P&M Invest”.
Взаимодействие индола и N-метилиндола с альдегидами
Синтез 2,2,3,3,3-пентафтор-1-(1H-индол-3-ил)пропан-1-ола, 1a
Типовая методика
К 1,0 мл предварительно охлажденного 1М раствора индола в ДХМ в атмосфере аргона добавляли 1,0 мл также охлажденного 1М раствора 2,2,3,3,3-пентафторпропаналя в смеси ДХМ-гексан (1:1), полученный раствор оставляли при -15оС на 6 дней. Ход реакции контролировали методом ТСХ (силикагель, элюент – ДХМ). Полученную смесь 1a и побочного продукта 3,3'-(2,2,3,3,3-пентафторпропан-1,1-диил)-бис-1H-индола (2a) разделяли методом хроматографии на колонке (элюент - ДХМ). После удаления растворителя получено 011 г 1a в виде желтой вязкой жидкости, выход 41%. 1Н ЯМР (dmso-d6, , ppm): 5,46 (дт, 1H, J1 = 20,35 Гц, J2 = 5,81 Гц, CH(OH)); 6,55 (д, 1H, J = 5,09 Гц, CH(OH)); 7,04 (т, 1H, J = 7,31 Гц, Ind-H); 7,12 (т, 1H, J = 7,31 Гц, Ind-H); 7,42 (д, 1H, J = 8,27 Гц, Ind-H); 7,50 (д, 1H, J = 2,54 Гц, Ind-H); 7,68 (д, 1H, J = 7,95 Гц, Ind-H); 11,28 (с, 1H, NH). 19F ЯМР (dmso-d6, , ppm): -49,97 (д, 1F, J = 268,55 Гц, А часть АВ-системы, CF2); -40,85 (д, 1F, J = 268,55 Гц, B часть АВ-системы, CF2); -2,02 (с, 3F, CF3).
Продукт 2a выделен в виде желтой жидкости. 1Н ЯМР (dmso-d6, , ppm): 5,51 (т, 1H, J = 19,17 Гц, CH(C2F5)); 7,01 (т, 2H, J = 7,32 Гц, Ind-H); 7,08 (т, 2H, J = 7,32 Гц, Ind-H); 7,36 (д, 2H, J = 8,04 Гц, Ind-H); 7,58 (д, 2H, J = 2,03 Гц, Ind-H); 7,74 (д, 2H, J = 7,83 Гц, Ind-H); 11,18 (с, 1H, NH). 19F ЯМР (dmso-d6, , ppm): -36,12 (с, 2F, CF2); -1,97 (с, 3F, CF3). MS (EI-DIP), m/z: 121,9; 218,1; 245,0; 363,9.
Соединения 1b,с и 3а-с, полученные аналогично, представляют собой твердые вещества белого или бледно-желтого цвета. Время реакций - от 1 дня (для 1b и 3b-c) до 4 или 6 дней для 1с и 3а соответственно. В процессе реакции продукты постепенно выпадают в осадок.
1b (1-H-перфтор-1-(1H-индол-3-ил)пентан-1-ол): время реакции – 1 день. Получено 0,25г мелкокристаллического белого порошка, выход 69%. 1Н ЯМР (dmso-d6, , ppm): 5,53 (дт, 1H, J1 = 21,36 Гц, J2 = 5,85 Гц, CH(OH)); 6,54 (д, 1H, J = 4,83 Гц, CH(OH)); 7,04 (т, 1H, J = 7,12 Гц, Ind-H); 7,12 (т, 1H, J = 7,12 Гц, Ind-H); 7,42 (д, 1H, J = 7,88 Гц, Ind-H); 7,50 (д, 1H, J = 2,29 Гц, Ind-H); 7,67 (д, 1H, J = 7,88 Гц, Ind-H); 11,28 (с, 1H, NH). 19F ЯМР (dmso-d6, , ppm): -47,29 (м, 3F, CF2CF2); -44,57 (д, 1F, J = 296,2 Гц, А часть АВ-системы, CF2); -42,74 (д, 1F, J = 296,2 Гц, B часть АВ-системы, CF2); -38,03 (д, 1F, J = 275,25 Гц, А часть АВ-системы, CF2); -2,28 (с, 3F, CF3). MS (EI-DIP), m/z: 69,1; 91,1; 118,0; 131,0; 145,9; 150,9; 177,9; 328,0; 346,9; 364,9; 393,9.
1c (1,7-2H-перфтор-1-(1H-индол-3-ил)гептан-1-ол): время реакции – 4 дня. Получено 0,2 г белого порошка, выход 45%. 1Н ЯМР (dmso-d6, , ppm): 5,51 (дм, 1H, J = 21,00 Гц, CH(OH)); 6,50 (д, 1H, J = 4,77 Гц, CH(OH)); 6,99-7,35 (м, 3H, Ind-H и CF2H); 7,41 (д, 1H, J = 8,01 Гц, Ind-H); 7,49 (м, 1H, Ind-H); 7,66 (д, 1H, J = 7,63 Гц, Ind-H); 11,27 (с, 1H, NH). 19F ЯМР (dmso-d6, , ppm): -60,47 (д, 1F, J = 310,67 Гц, А часть АВ-системы, CF2H); -59,97 (д, 1F, J = 310,67 Гц, B часть АВ-системы, CF2H); -50,95 (с, 2F, CF2CF2H); -45,87 (д, 1F, J = 274,93 Гц, А часть АВ-системы, CF2C(OH)); -44,93 (д, 2F, J = 145,71 Гц, CF2); -43,76 (д, 2F, J = 118,22 Гц, CF2); -42,69 (д, 2F, J = 129,22 Гц, CF2); -37,91 (д, 1F, J = 274,93 Гц, B часть АВ-системы, CF2C(OH)). MS (EI-DIP), m/z: 91,1; 117,0; 118,0; 145,9; 150,9; 177,9; 189,9; 428,8; 446,7.
3a (2,2,3,3,3-пентафтор-1-(1-метилиндол-3-ил)пропан-1-ол): время реакции – 6 дней. Получено 0,18 г бледно-желтого пушистого порошка, выход 65%. 1Н ЯМР (dmso-d6, , ppm): 3,81 (с, 3H, CH3); 5,46 (дт, 1H, J1 = 20,60 Гц, J2 = 6,10 Гц,CH(OH)); 6,58 (д, 1H, J = 5,34 Гц, CH(OH)); 7,08 (т, 1H, J = 7,88 Гц, Ind-H); 7,19 (т, 1H, J = 7,88 Гц, Ind-H); 7,45 (д, 1H, J = 8,39 Гц, Ind-H); 7,49 (м, 1H, Ind-H); 7,68 (д, 1H, J = 7,88 Гц, Ind-H). 19F ЯМР (dmso-d6, , ppm): -50,13 (д, 1F, J = 268,55 Гц, CF2); -40,72 (д, 1F, J = 268,55 Гц, CF2); -1,98 (с, 3F, CF3). MS (EI-DIP), m/z: 117,0; 132,0; 159,9; 278,8.
3b (1-H-перфтор-1-(1-метилиндол-3-илl)пентан-1-ол): время реакции – 1 день. Получено 0,2 г бледно-желтого пушистого порошка, выход 53%. 1Н ЯМР (dmso-d6, , ppm): 3,81 (с, 3H, CH3); 5,52 (д, 1H, J = 21,11 Гц, CH(OH)); 6,57 (с, 1H, CH(OH)); 7,07 (т, 1H, J = 7,51 Гц, Ind-H); 7,19 (т, 1H, J = 7,50 Гц, Ind-H); 7,45 (д, 1H, J = 8,39 Гц, Ind-H); 7,50 (с, 1H, Ind-H); 7,67 (д, 1H, J = 7,63 Гц, Ind-H). 19F ЯМР (dmso-d6, , ppm): -51,12 – -48,28 (м, 3F, CF2CF2); -46,93 (д, 1F, J = 296,02 Гц, А часть АВ-системы, CF2); -45,19 (д, 1F, J = 296,02 Гц, B часть АВ-системы, CF2); -40,43 (д, 1F, J = 277,71 Гц, А часть АВ-системы, CF2); -4,70 (с, 3F, CF3). MS (EI-DIP), m/z: 117,0; 132,0; 159,9; 223,9; 343,0; 378,8.
3c (1,7-2H-перфтор-1-(1-метилиндол-3-ил)гептан-1-ол): время реакции – 1 день. Получено 0,27 г белого плотного порошка, выход 59%. 1Н ЯМР (dmso-d6, , ppm): 3,80 (с, 3H, CH3); 5,51 (д, 1H, J = 20,35 Гц, CH(OH)); 6,54 (с, 1H, CH(OH)); 6,97-7,35 (м, 3H, Ind-H и CF2H); 7,45 (д, 1H, J = 8,27 Гц, Ind-H); 7,50 (с, 1H, Ind-H); 7,67 (д, 1H, J = 7,63 Гц, Ind-H). 19F ЯМР (dmso-d6, , ppm): -60,47 (д, 1F, J = 312,81 Гц, А часть АВ-системы, CF2H); -59,95 (д, 1F, J = 312,81 Гц, B часть АВ-системы, CF2H); -50,92 (с, 2F, CF2CF2H); -45,95 (д, 1F, J = 276,19 Гц, А часть АВ-системы, CF2C(OH)); -44,91 (д, 2F, J = 146,48 Гц, CF2); -43,75 (д, 2F, J = 122,07 Гц, CF2); -42,65 (д, 2F, J = 128,17 Гц, CF2); -37,83 (д, 1F, J = 276,19 Гц, B часть АВ-системы, CF2C(OH)). MS (EI-DIP), m/z: 116,9; 132,0; 159,9; 160,9; 460,8.
Взаимодействие индола с метиловой полуацеталью перфторпропаналя
Синтез 2,2,3,3,3-пентафтор-1-(1H-индол-3-ил)пропан-1-ола, 1a
К 1,0 мл 1 М раствора индола в ДХМ в атмосфере аргона добавляли 1,0 мл 1М раствора метиловой полуацетали перфторпропаналя в смеси ДХМ-гексан (1:1), полученный раствор оставляли при комнатной температуре в закрытом от света сосуде на 4 дня. Ход реакции контролировали методом ТСХ (силикагель, элюент – ДХМ). Растворитель удаляли в вакууме, продукт 1а выделяли методом хроматографии на колонке (силикагель, элюент - ДХМ). Выход 0,04г (15%).
При проведении соответствующей реакции (индол : полуацеталь = 1 : 2) в запаянной ампуле, закрытой от света, при температуре 45˚С в течение 30 часов после аналогичной обработки получено 0,12 г 1a (выход 45% отн. индола) и 0,09 г 2a (выход 49% отн. индола).
Список литературы
- Katayama, M.; Gautam, R. K. Biosci. Biotechnol. Biochem. 1996, 60 (5), 755–759.
- Török, B.; Sood, A.; Bag, S.; Kulkarni, A.; Borkin, D.; Lawler, E.; Dasgupta, S.; Landge, S.; Abid, M.; Zhou, W.; Foster, M.; Levine, H.; Török, M. ChemMedChem 2012, 7 (5), 910–919.
- Satoh, A.; Nishina, Y. Cell-death inhibitor, and novel compound containing indole compound or benzoxazole compound, and preparation thereof. WO2014136808 A1, September 12, 2014
- Sayed, M. T. El; Ahmed, K. M.; Mahmoud, K.; Hilgeroth, A.; El Sayed, M. T.; Ahmed, K. M.; Mahmoud, K.; Hilgeroth, A. Eur. J. Med. Chem. 2015, 90, 845–859.
- Yao, S. J.; Ren, Z. H.; Wang, Y. Y.; Guan, Z. H. J. Org. Chem. 2016, 81 (10), 4226–4234.
- Vitaku, E.; Smith, D. T.; Njardarson, J. T. Angew. Chemie - Int. Ed. 2016, 55 (6), 2243–2247.
- Kucher, O. V.; Kolodiazhnaya, A. O.; Smolii, O. B.; Prisuazhnyk, D. V.; Tolmacheva, K. A.; Zaporozhets, O. A.; Moroz, Y. S.; Mykhailiuk, P. K.; Tolmachev, A. A. European J. Org. Chem. 2014, 2014 (34), 7692–7698.
- Dong, J.; Pan, L.; Xu, X.; Liu, Q. Chem. Commun. 2014, 50 (94), 14797–14800.
- Kosobokov, M. D.; Levin, V. V; Struchkova, M. I.; Dilman, A. D. Org. Lett. 2014, 16 (14), 3784–3787.
- Borkin, D. A.; Landge, S. M.; Török, B. Chirality 2011, 23 (8), 612–616.
- Gong, Y.; Kato, K. J. Fluor. Chem. 2001, 108 (1), 83–86.
- Mitchell, L.; Williamson, P.; Ehrlichov, B.; Anderson, A. E.; Seymour, V. R.; Ashbrook, S. E.; Acerbi, N.; Daniels, L. M.; Walton, R. I.; Clarke, M. L.; Wright, P. A. Chem. - A Eur. J. 2014, 20 (51), 17185–17197.
- Xu, Z.; Hang, Z.; Chai, L.; Liu, Z.-Q. Org. Lett. 2016, 18 (18), 4662–4665.
- Landge, S. M.; Borkin, D. A.; Török, B. Tetrahedron Lett. 2007, 48 (36), 6372–6376.
- Maki, Y.; Kimoto, H.; Fujii, S.; Senga, M.; Cohen, L. A. J. Fluor. Chem. 1988, 39 (1), 47–59.
Статья рекомендована к публикации членом редколлегии д.х.н. Н.Д. Чканиковым
Fluorine Notes, 2017, 113, 1-2


