Поступило в редакцию: ноябрь 2014
УДК 547.464.6; 547.433; 535.32; 535.34
Fluorine Notes, 2014, 97, 7-8
Синтез и оптические характеристики пергалогенированныхтрет-бутил-альфа-фторакрилатов
A.A. Тютюновabc, В.Э. Бойкоabc, А.В. Синькоabc, С.М. Игумновabc, С.И. Молчановаc, Е.В. Хайдуковc, В.И. Соколовc
aИнститут элементоорганических соединений им. А.Н. Несмеянова Российской академии наук, Российская
Федерация, 119991 Москва, ул. Вавилова, 28.
e-mail: tuytuynov@rambler.ru
bНПО “ПиМ-Инвест”, 119991, Москва, ул. Вавилова, д. 28
сИнститут проблем лазерных и информационных технологий РАН, ул. Святоозерская, д. 1, 140700, Шатура, Моск. обл., Россия
Аннотация. Синтезированы новые пергалогенированные трет-бутил-альфа-фторакрилаты вида CH2=CFCO2R, где R = (CF3)3C, CF2Cl(CF3)2C, CF3(CF2Cl)2C. Измерены их спектры поглощения и рефракции в телекоммуникационных областях длин волн вблизи 0.85, 1.3 и 1.55 мкм. Показано, что коэффициент поглощения мономеров при 1.55 мкм не превышает 0.1 дБ/см, показатель преломления лежит в пределах 1.2990–1.3586.
Ключевые слова: Альфа-фторакрилаты, коэффициент поглощения, показатель преломления.
Оптические устройства на основе полимерных материалов представляют значительный интерес для создания высокоскоростных линий передачи данных [1-2]. Среди всего разнообразия полимеров, предложенных для изготовления таких устройств, полиакрилатам уделяется особое внимание. Это связанно как с простотой синтеза и модификации акриловых мономеров, так и с их способностью полимеризоваться под действием УФ излучения, что делает возможным использовать их для создания интегрально-оптических устройств методами фотолитографии и прямого лазерного рисования [3-5].
Полиакрилаты, использующиеся для изготовления светопроводящих жил и оболочки оптических волноводов, должны иметь высокую температуру стеклования (Тs > 110oC), термическую стабильность (Тd > 200°С), оптическую прозрачность (< 0.07 дБ/см вблизи 1.55 мкм), незначительные изменения показателя преломления с ростом температуры (dn/dT < 5.10-5), механическую прочность и в тоже время гибкость, стабильность к воздействию окружающей среды [6-9]. Для получения полимеров с такими характеристиками используют различные метакрилаты или α-фторакрилаты, содержащие в эфирной части молекулы полигалогенированные алкильные и/или арильные группы [10-22].
Известно, что наиболее высокой оптической прозрачностью в телекоммуникационных областях длин волн обладают полимеры с наименьшим содержанием связей C-H [4-5, 8-9, 11]. Очевидно, что среди акриловых мономеров, эфиры α-фторакриловой кислоты, полученные на основе пергалогенированных третичных спиртов, представляют особый интерес для получения полиакрилатов, имеющих максимально высокую оптическую прозрачность и максимально высокую фотополимеризационную активность среди полимеров данного типа. Целью данной работы являлась разработка методов синтеза ранее неописанных пергалогенированных трет-бутил-α-фторакрилатов и определение их оптических характеристик.
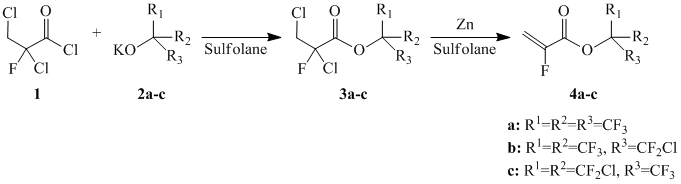
Синтез α-фторакрилатов 4a-c осуществлен по методу [7] реакцией хлорангидрида (1) c алкоголятами третичных спиртов 2а-с с последующим дехлорированием образующихся сложных эфиров 3а-с (см. Схему 1):
Схема 1
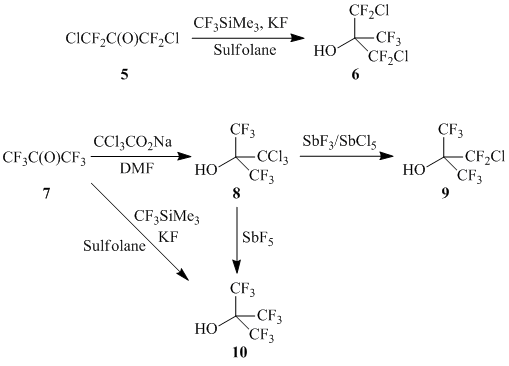
Спирты 6, 9, 10 были описаны ранее [23-24]; схема их получения приведена ниже (см. Схему 2):
Схема 2
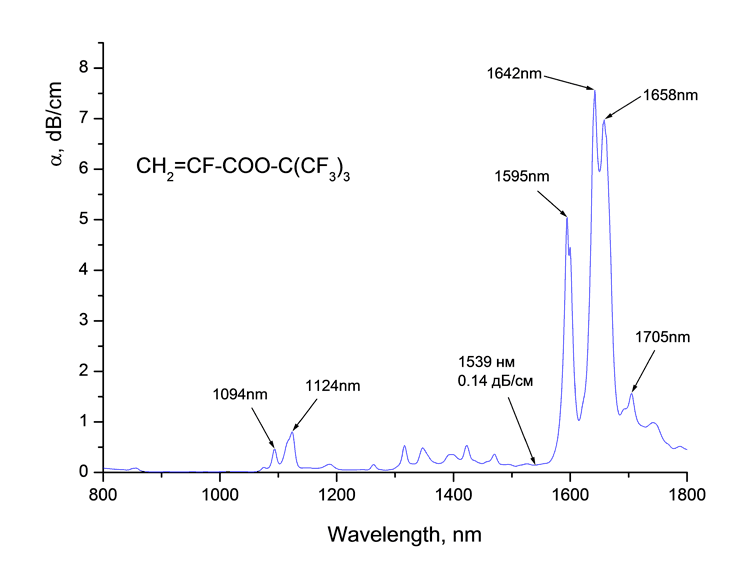
Спектры поглощения синтезированных мономеров в телекоммуникационных диапазонах длин волн вблизи 0.85, 1.3 и 1.55 мкм, измеренные на спектрофотометре Shimadzu UV3600, представлены на Рис. 1. В спектрах наблюдаются полосы поглощения, а также окна прозрачности. Коэффициент поглощения мономеров вблизи 1.55 мкм составляет 0.1 дБ/см.
|
|
|
|
|
|
Рис. 1. Спектры поглощения мономеров CH2=CF-CO2C(CF3)3 (а), CH2=CF-CO2C(CF2Cl)(CF3)2 (б) и CH2=CF-CO2C(CF2Cl)2(CF3)
(в) вблизи 1.55 мкм.
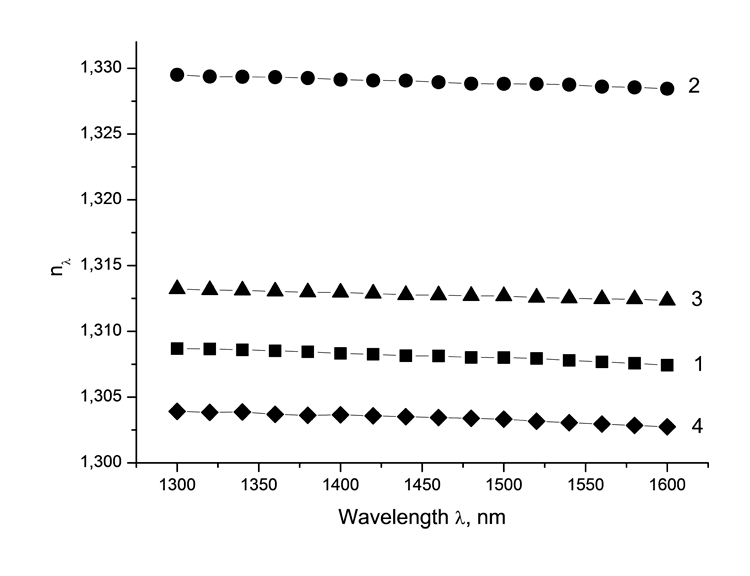
Дисперсионные зависимости показателя преломления мономеров измерены на созданном в ИПЛИТ РАН спектроскопическом рефрактометре [25], см. Рис. 2. Мономеры имеют нормальную дисперсию, их показатель преломления на длине волны λ=1.55 мкм составляет 1.2990 (4a), 1.3288 (4b) до 1.3586 (4c), и повышается с увеличением числа атомов хлора.
|
|
Рис. 2. Показатели преломления nλ галогенированных акриловых мономеров CH2=CF-CO2C(CF3)3 (1), CH2=CF-CO2C(CF2Cl)(CF3)2 (2), CH2=CF-CO2C(CF2Cl)2CF3 (3) в ближней ИК области спектра, измеренные при 20oC.
Синтезированные мономеры способны к радикальной фотополимеризации и пленкообразованию. Они могут быть использованы для формирования полимерных волноводов и других элементов интегрально-оптических устройств методами контактной УФ фотолитографии и прямого лазерного рисования.
Экспериментальная часть
ЯМР 1H, 19F спектры записаны на спектрометре “Bruker AVANCE-300” при 300 и 282 MHz, соответственно, внешний стандарт CDCl3. Химические сдвиги для 1H спектров приведены относительно остаточного сигнала растворителя (δ 7.26) и даются в м.д. относительно ТМС. Химические сдвиги спектров 19F приведены в м.д. относительно CFCl3. Слабопольные сдвиги имеют положительное значение.
Синтез соединений 1, 6, 9, 10 описан ранее [7, 23-24]. Алкоголяты третичных спиртов 2a-c получены по известному методу [26].
Сложные эфиры 3a-c получены взаимодействием хлорангидрида 1 с алкоголятами 2a-c в сульфолане при 20-50°С, с последующей отгонкой продукта реакции из реакционной смеси в вакууме 10-15 Торр и дополнительной очисткой 3a-c перегонкой.
1,1,1,3,3,3-Гексафтор-2-(трифторметил)пропан-2-ил 2,3-дихлор-2-фторпропаноат (3a). Т.кип. 50-52°С(15 Торр). ЯМР 1H δ: 4.0÷4.2 (м, CH2Cl); ЯМР 19F δ: -125.4 (м, 1F, CFCl), -71.7 (м, 9F, CF3).
1-Хлор-1,1,3,3,3-пентафтор-2-(трифторметил)пропан-2-ил 2,3-дихлор-2-фторпропаноат (3b). Т.кип. 67-68°С(10 Торр). ЯМР 1H δ: 3.8÷4.1 (м, CH2Cl); ЯМР 19F δ: -125.4 (м, 1F, CFCl), -70.0 (с, 6F, CF3), -59.5 (с, 2F, CF2Cl).
1,3-Дихлор-1,1,3,3-тетрафтор-2-(трифторметил)пропан-2-ил 2,3-дихлор-2-фторпропаноат (3c). Т.кип. 200-205°С. ЯМР 1H δ: 3.8÷4.1 (м, CH2Cl); ЯМР 19F δ: -124.5 (м, 1F, CFCl), -67.2 (м, 3F, CF3), -56.8 (м, 4F, CF2Cl).
Общий метод синтеза пергалогенированных трет-бутил-α-фторакрилатов 4a-c.
К суспензии цинковой пыли (9.81 г, 0.15 г-атом) активированной добавлением триметилхлорсилана (1 мл) в сульфолане (50 мл) в вакууме 10-15 Торр при перемешивании и температуре 30-40°С по каплям добавляется сложный эфир 3a-c (0.1 моль), продукт реакции отгоняется в охлаждаемый до 0°С приемник. Полученный продукт дополнительно очищается ректификацией в вакууме 10-15 Торр. Выход очищенного продукта 70-75%. Чистота полученных мономеров по ГЖХ составляет 98-99%.
1,1,1,3,3,3-Гексафтор-2-(трифторметил)пропан-2-ил 2-фторакрилат (4a). CH2=CFCO2C(CF3)3. Т.кип. 19-20°С(15 Торр). ЯМР 1H δ: 5.7÷6.2 (м, CH2=); ЯМР 19F δ: -119.4 (м, 1F, CFCl), -71.7 (м, 9F, CF3).
1-Хлор-1,1,3,3,3-пентафтор-2-(трифторметил)пропан-2-ил 2-фторакрилат (4b). CH2=CFCO2C(CF3)2CF2Cl. Т.кип. 33.5-34°С(10 Торр). ЯМР 1H δ: 5.5÷6.0 (м, CH2=); ЯМР 19F δ: -118.7 (м, 1F, CF), -69.6 (м, 6F, CF3), -59.1 (м, 2F, CF2Cl).
1,3-Дихлор-1,1,3,3-тетрафтор-2-(трифторметил)пропан-2-ил 2-фторакрилат (4c). CH2=CFCO2C(CF2Cl)2CF3. Т.кип. 62.5-63°С(10 Торр). ЯМР 1H δ: 5.5÷6.0 (м, CH2=); ЯМР 19F δ: -118.2 (м, 1F, CF), -67.1 (м, 3F, CF3), -56.7 (м, 4F, CF2Cl).
Благодарности
Работа выполнена при финансовой поддержке гранта Российского Научного Фонда (РНФ) 14-19-01659.
Список литературы
- W. Daum, J. Krauser, P.E. Zamzow, O. Ziemann. POF – polymer optical fibers for data communication. ISBN 3-540-42009-6, Springer-Verlag Berlin Heidelberg New York, 2002.
- O. Ziemann, J. Krauser, P.E. Zamzow, W. Daum. POF Handbook – Optical Short Range Transmission Systems. 2nd Edition. ISBN 978-3-540-76628-5, Springer-Verlag Berlin Heidelberg, 2008.
- H. Ma, A.K.-Y. Jen, L.R. Dalton Adv. Mater., 2002, 14, 1339-1365.
- M. Zhou Optical Engineering, 2002, 41, 1631-1643.
- Y. Koike, K. Koike J.Pol.Sci: Part B: Pol.Phys., 2011, 49, 2-17.
- T. Kaino, Y. Katayama Pol.Engin. and Sci., Mid-Sept., 1989, 29, 1209-1214.
- L.S. Boguslavskaya, I.Yu. Panteleeva, T.V. Morozova, A.V. Kartashov, N.N. Chuvatkin Russ.Chem.Rev., 1990, 59, 906-917.
- B. Boutevin, A. Rousseau, D. Bosc J.Pol.Sci: PartA: Pol.Chem., 1992, 30, 1279-1286.
- A. Rousseau, B. Boutevin AIP Conf.Proc., 2004, 709, 214-232.
- Japan Patent 1974, №49-129545.
- T. Kaino J.Pol.Sci.: Part A: Pol.Chem., 1987, 25, 37-46.
- T. Sakagami, N. Murayama US Patent 1988, №4,775,590.
- H. Teng, L. Yang, F. Mikes, Y. Koike, Y. Okamoto Polym.Adv.Technol., 2007, 18, 453-457.
- A. Tagaya, T. Harada, K. Koike, Y. Koike, Y. Okamoto, H. Teng, L. Yang J.Appl.Pol.Sci., 2007, 106, 4219-4224.
- D. Zhou, H. Teng, K. Koike, Y. Koike, Y. Okamoto J.Pol.Sci.: Part A: Pol.Chem., 2008, 46, 4748-4755.
- K. Koike, F. Mikes, Y. Koike, Y. Okamoto Polym.Adv.Technol., 2008, 19, 516-520.
- K. Koike, F. Mikes, Y. Okamoto, Y. Koike J.Pol.Sci.: Part A: Pol.Chem., 2009, 47, 3352-3361.
- K. Koike, T. Kado, Z. Satoh, Y. Okamoto, Y. Koike Polymer, 2010, 51, 1377-1385.
- J.-M. Cracowski These Docteur, Universite du Maine, U.F.R. Sciences et Techniques, 2008.
- J.-M. Cracowski, V. Montembault, I. Hardy, D. Bosc, B. Ameduri, L. Fontaine J.Pol.Sci: Part A: Pol.Chem., 2008, 46, 4383-4391.
- J.-M. Cracowski, V. Montembault, D. Bosc, B. Ameduri, F. Odobel, L. Fontaine J.Pol.Sci:PartA:Pol.Chem., 2009, 47, 1403-1411.
- W. Yao, Y. Li, X. Huang Polymer, 2014, http://dx.doi.org/10.1016/j.polymer.2014.09.036.
- R.E.A. Dear Synthesis, 1970, 361-362.
- Yu.V. Zeifman Bull.Russ.Acad. of Sci., Div. of chem. sci., 1992, 41, 370-373.
- V.I. Sokolov, M.S. Kitai, G.V. Mishakov, S.I. Molchanova, V.Ya. Panchenko, I.V. Sokolova PTE, 2011, 157-158.
- F.J. Pavlik US Patent 1972, №3668233A.
Статья рекомендована к публикации членом редколлегии проф. С.Р. Стерлиным
Fluorine Notes, 2014, 97, 7-8
 а)
а)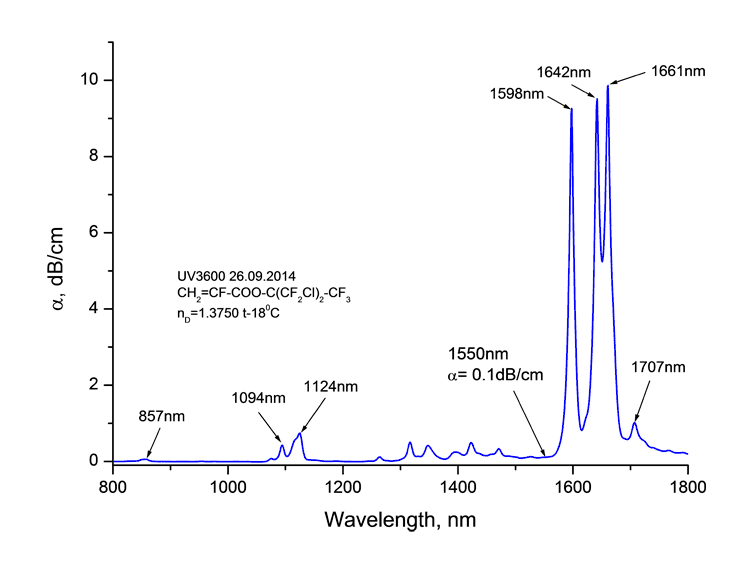 b)
b)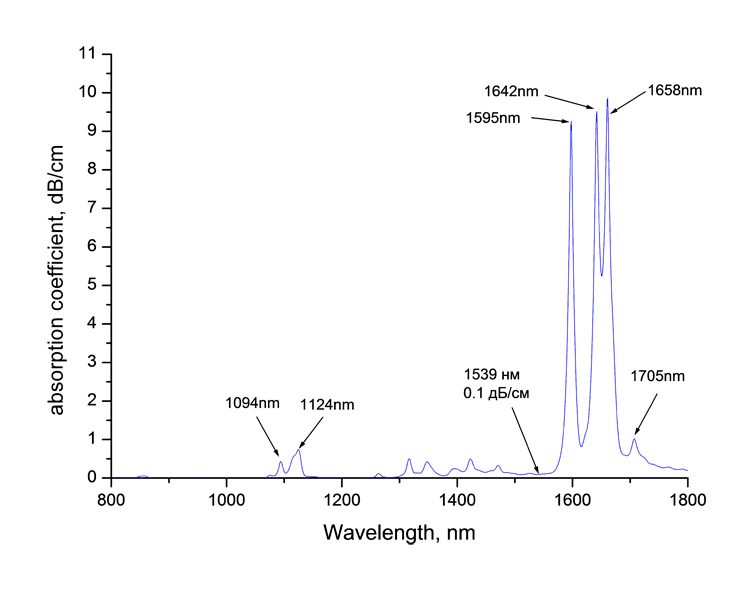 c)
c)